細胞株の構築
最近のバイオ医薬品の生産細胞株構築フローを以下に示します。
- Host Cell : 目的のタンパク質を発言させるために使用する出発材料である最適化された細胞。目的遺伝子を導入する予定の細胞。
- Transfection : 遺伝子の導入プロセス
- Selection & Cloning : 高い生産性と増殖による世代安定性を維持するモノクローンを選択するプロセス
- Cell Bank : Master Cell Bank (MCB)の候補となる細胞株
- MCB : 品質試験されて正式に決定した生産細胞株(Characterized Cell Bankという言い方もある)
- Working Cell Bank (WCB) : Expanded MCB/マスターセルバンクの拡大培養により細胞を増やして、MCBと土曜用に品質試験されて正式に決定した生産細胞株。ルーチン製造に使用される。
導入遺伝子の構築
- gene配列の合成
- Plasmid DNAの合成
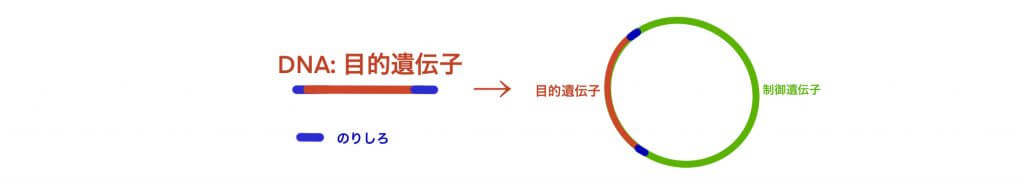
制御遺伝子には、Promoter、Enhancer などがあり、高い生産性を目的とする。抗生物質耐性遺伝子は、目的遺伝子が正しく細胞に導入された場合、それと共に発現するため、抗生物質を添加した培地でも生き延びることが可能となる。遺伝子が導入できなかった細胞は、死滅させることができる。
遺伝子導入とは
遺伝子の導入 (transfection)するの目的は、ある細胞に目的遺伝子を導入(Transfection)することで、宿主細胞の力を借りて、その遺伝子にコードされている蛋白質を生産させることである。
どんな細胞を使うか
一般的に通常の細胞は寄り添います。たとえば、皮膚細胞は、それぞれの細胞は積み上がることなく横に広がる性質があります( monolayer cell ).
バイオ医薬品に使用される細胞は、1個1個の細胞が単独で浮遊するように改良が加えられており、細胞の培養において、個々の細胞に栄養分が均一に行き渡らせることが可能です。コントロールしやすい細胞になっています。
長い歴史の中で、HEK細胞、CHO細胞などが、遺伝子導入する細胞として適しているとして多くのバイオロジクスで使用されています。

原材料
細胞とPlasmid DNAについて
- 1個の細胞を使って1のPlasmid DNAを、その細胞に導入できる技術は、世の中にはありません。
- 細胞もPlasmid DNAも物理化学的に不安定な部類です。人工的な処理やある環境下では、一定の確立で死ぬか壊れてしまいます。
- 実際の導入には、細胞やPlasmidが、死ぬか壊れるかを考慮し、確実に細胞に遺伝子を導入するために、細胞数として数十万個、あるいは数百万個を用意します。
- 細胞の中に導入したいPlasmid DNAも細胞に対して等倍はあり得ず、複数倍を用意します。経験則も存在します。
導入 ( Transfection )
導入法の種類
- リン酸カルシウム
- リン酸カルシウム溶液とPlasmid DNA複合微粒子を細胞に混和すると、プラス荷電化によりマイナス荷電している細胞膜表面に結合し、その後、エンドサイトーシス機構で取り込まれる
- リン酸カルシウム溶液とPlasmid DNA複合微粒子を細胞に混和すると、プラス荷電化によりマイナス荷電している細胞膜表面に結合し、その後、エンドサイトーシス機構で取り込まれる
- 陽イオン性脂質 (lipofection*1)
- Plasmid DNAを包含したリン脂質と細胞膜が膜融合する原理で導入する
- 試薬 ThermoFisher
- マグネットフェクション (magnetofection)
- 作製した磁気ナノパーティクルとPlasmid DNAの結合物を、底に沈めた細胞がある容器に注入し、細胞へ向かうように容器の下から磁気をかけて導入する
- 試薬 funakoshi
- エレクトロポレーション (electroporation)
- エレクトロトランスポレーターを使用して電気のパルスをかけて細胞膜に小さな穴を開けてPlasmid DNAを導入する
- 装置 参考記事*
- ウイルス (virus vector)
- 原理的にはLipofectionと類似。包含体としてのキャリアとしてウイルスを使われる。retrovirusなどが使われる