mRNAワクチンとは
mRNAワクチンは、核酸医薬であり、核酸のモダリティに分類される。モダリティは、手段を意味しているので、以下のようなものが考えられます。
- 低分子合成品
- タンパク質
- 核酸
- ウイルス (AAV, Lentivirus, Adenovirus)ベクター
mRNAワクチンの優位性
mRNAの優位性について、COVID-19ワクチンとしてTranslate Bio社とmRNAを使って共同開発しているSanofi社のサイトから引用 source
- 核への侵入を必要とせずにタンパク質生産を開始できる
- DNAワクチンの場合は、核に入って、mRNAに転写させる必要がありますが、mRNAは、細胞質内でRibosomeによってタンパク質への翻訳が可能です
- 迅速な開発が可能
- タンパク質ベースやその他モダリティよりは、IT技術を駆使できれば迅速な開発は可能と思われます
- 非ウイルスを使用した低コストの製造と安全な投与
- 従来の生ワクチンや弱毒ワクチンなどと比較して、全くの無生物であること、それらに比べれば製造ステップは少なくてすみます
以下に、mRNAについて文献の内容から概説1)します。
mRNAワクチンは、体内に直接投与する。mRNAはタンパク質をコードする核酸であり、細胞質内に入り込むことができれば、細胞の機能を利用して、コードしたタンパク質が作られる。しかし、RNAは非常に分解されやすいため、医薬品化を達成した品目はない。DNAでは、染色体への相同組換の危険性を伴うが、mRNAではその危険性は全くない。
歴史的経緯
核酸医薬としての最初の報告は、1990年のScience論文です。動物の骨格筋に投与した実験例は2つ実施されました。
- プラスミドDNS (pDNA)
- mRNA
当初、適切な遺伝子導入試薬を使えば、培養細胞へのpDNAおよびmRNAを細胞に導入(in vitro)することができ、その結果、タンパク質を作らせることができた。しかし、動物の骨格筋への導入(in vivo)では、mRNAでは、タンパク質を作らせることができませんでした。その原因は、mRNAが生体内では、非常に不安定であるためでした。
最近のmRNAに関する研究・開発の成果は、アメリカ、ドイツが中心のようです。日本も頑張って欲しいと思います。
mRNAを医薬にするためには
- ARCA法 (anti-reverse cap analogues)の開発*1)
- コドン最適化
- 世界は、ITを駆使している分野です。ITが弱い日本で勝機があるのか疑問です。
- 免疫原性の制御 (メチル化核酸、シュードウリジン、などは、非開示のものも多い)
*1) DNA鋳型としてmRNAが作られますが、次ステップのmRNAからタンパク質をつくるには、mRNA5’末端にcap構造が必要であるため、mRNAにcapアナログを付加しなければ、医薬品にはなりません。しかし、cap構造の人工的な付加は、効率が低く50%程度でした。更に詳しくは、別文献を参照2)のこと。次章で述べていますが、これまでの研究では、Capの不要化も検討されているようです。
編集履歴 2020/05/03 はりきり(Mr) 2020/05/15 追記 (moderna社が先行するmRNAワクチン) 2020/05/23 追記 (CleanCap法) 2020/09/29 追記 (モダリティ) 2020/10/22 追記 (mRNAワクチンの優位性 ~ Sanofiサイトより引用)
mRNA医薬の構造
医薬品に仕上げるために行われた、重要な研究項目について、以下に示されています。図には、mRNA構造が示されています。翻訳領域であるORF3)と比較して、非翻訳領域である5’UTR, 3’UTRの配列4)の改変は、比較的自由度があります。
1. 5’ Cap
- Capの不要化
- 5’Capの一般的な機能wiki
- 核外輸送
- 5’-3’エキゾタクレアーゼ抵抗性と分解抵抗性
- 翻訳促進
- イントロンのスプライシング促進
2. 5’ UTR/3’ UTR
- mRNA輸送・翻訳など
3. DRF
- 翻訳効率
- 分解耐性
4. Poly A
- mRNA安定化
5. mRNA全体
- 免疫原性の低減化
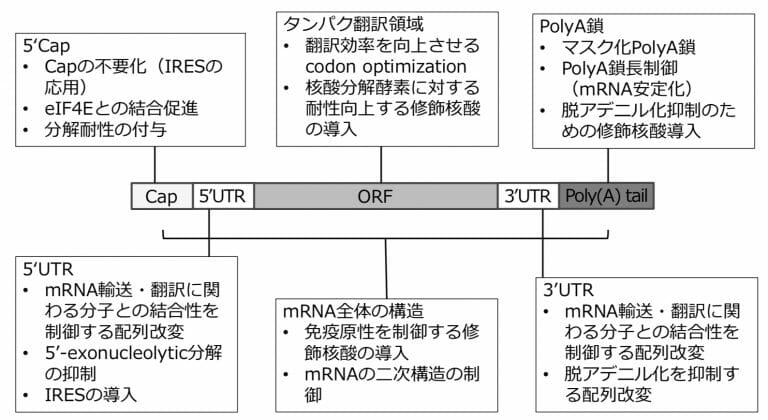
図1. 治療用mRNAの構造
参考文献1), p.454参照。
mRNA医薬の方向性
mRNA医薬は、広義の遺伝子治療の範疇であるが、ホスト細胞のゲノムへの取り込みがないことは、大きなメリットである。そのため、比較的一般的な治療にも適用が考えられる。
- ワクチン
- Moderna (US)
- BioNTech (ドイツ)
- CureVac (ドイツ)
- GSK
- 非遺伝性の疾患全般
- 加齢変性疾患
- 外傷
課題
- mRNAワクチン
- 皮下投与であるため高性能なDDSは必要ない
- 標的細胞へのDDS
- 脂質ナノ粒子 (LNP, 非開示): 炎症反応の惹起がある。
- ポリマー粒子: 組織浸透性が優れている
- 免疫反応の低減化
ワクチン
一般的に、DDS併用でない場合、免疫賦活化作用が十分ではない。部分的にmRNAの二本鎖構造にして、抗原提示能と免疫賦活作用を併せ持つmRNAの開発も行われている。
mRNAワクチンで先人を切っているのは、米国のmoderna社です。詳しくは、以下の記事をご覧ください。
がんワクチン
- 液性免疫と細胞性免疫に適用可能
- 2017年、BioNTechのメラノーマワクチン(new-antigen mRNAワクチン)
- PD-(L)1阻害剤 (免疫チェックポイント阻害剤)との併用。BioNTechは、Genentechと共同で臨床試験実施。CureVacはEli Lilly, ModernaはMerckと併用の臨床試験を実施。
一般治療
- 成長因子 (overdoseが抑制できる)
- VEGF mRNA (心虚血疾患、二型糖尿病皮下投与、アストラゼネカ)
- 組織再生(徐放): 軟骨、椎間板
- シグナル
- 非分裂成熟細胞(脳神経系など)
- 酵素
- 遺伝性稀少疾患(酵素補充)
- 膜タンパク質
特許
天然の核酸分子の配列では、特許は取れない。
以上
参考文献
1) mRNA 医薬開発の世界的動向, 医薬品医療機器レギュラトリーサイエンス
mRNA 医薬開発の世界的動向, 医薬品医療機器レギュラトリーサイエンス,PMDRS,50(5),242 ~ 249(2019)
http://nats.kenkyuukai.jp/images/sys/information/20190717095649-6ABC2FA50410294C82EBEF7D74463510333BCF1FB717B3F864612BCB0CA9F6B2.pdf
2) メッセンジャー RNA 医薬を実現する DDS 開発と疾患治療への応用
メッセンジャー RNA 医薬を実現する DDS 開発と疾患治療への応用、Drug Delivery System 31―4, 2016
https://www.jstage.jst.go.jp/article/dds/31/4/31_343/_pdf
3) ゲノム解析とは
ゲノム解析とは – nite – より
ORFは、開始コドンと呼ばれる3塩基から始まり、終止コドンと呼ばれる3塩基で終わります。また、アミノ酸に対応するコドンも解読されており、ORFの推定はコンピュータを用いて行います。
https://www.nite.go.jp/nbrc/genome/description/analysis2.html
4) 非翻訳領域
非翻訳領域 – wikipedia – より
https://ja.wikipedia.org/wiki/非翻訳領域
5) mRNAサーベイランスとは
mRNAサーベイランスとは、大野研究室 分子細胞生物学 Cell Signaling – より
http://www-user.yokohama-cu.ac.jp/~ohnos/research/mRNA.html