はじめに
目次
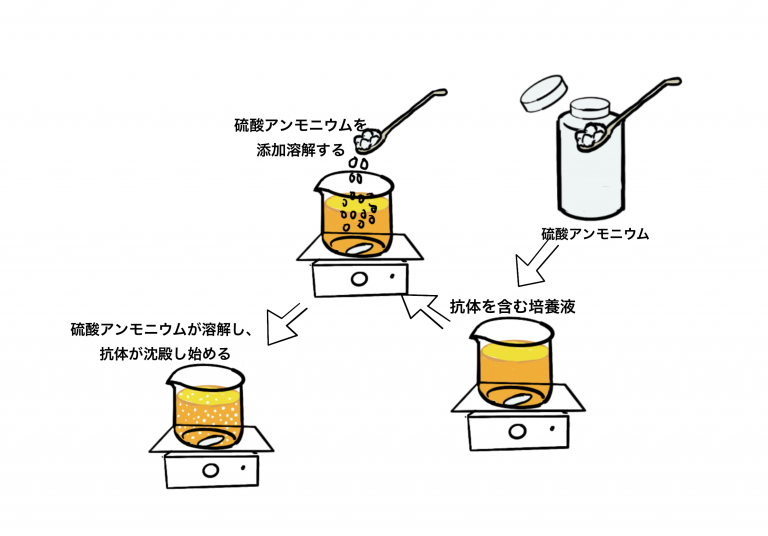
無機塩の高濃度添加は、タンパク質を沈殿させる基本です。タンパク質溶液に対して塩を添加することで、タンパク質の疎水性という物理的性質の強度を溶液中で強めることができます。疎水性が高まると、そのタンパク質の成分である疎水性のアミノ酸や疎水性の領域が、水を避けて互いにより集まり結合します。その性質の違いは、そのタンパク質固有のアミノ酸の含有比率に応じて、タンパク質毎に沈殿化する塩の種類、濃度、溶液pH、及び当該タンパク質のタンパク質濃度などの組み合わせに応じて重合化し、やがて沈殿化します。
- タンパク質濃度
- 沈殿とは分子同士が互いに寄り添い凝集することです。その基本原理からすると、沈殿させたいタンパク質の濃度が高いほど、沈澱しやすくなることは容易に理解できます。
- タンパク質の分子量
- 分子量が大きいほど、疎水性のアミノ酸の総数は一般論として多くなることは理解できます。すなわち、疎水性アミノ酸が増えるので沈殿になりやすいのです。
- タンパク質のアミノ酸組成の比率
- これは、上述のタンパク質の分子量から推定するよりは、直接的に評価できる指標です。ただし、分子の立体構造上で表面に出ている疎水性のアミノ酸として多いほどという条件も付きます。
- タンパク質のフォールディング(立体構造)の状況
- タンパク質のフォールディングの状態とはなんでしょうか。タンパク質は、基本的に1本のペプチドの鎖が、巻き、折畳まることで、その天然の立体構造としての状態になります。この状態が、最も血液に溶けやすくなっているのです。すなわち、疎水性のアミノ酸は内側に、親水性のアミノ酸は外側に配置されることになります。ミスフォールディングすると、その状態が不整合しているため疎水性アミノ酸が外側に多く出ている状態が起こり得て、そのため分子間での疎水性同士の結合インタラクショにより沈殿形成しやすくなります。
- 溶液のpH
- これは、私の経験則ですが、理由をよく考えると理解ができるものと思っています。ただ、今までよく考えて小なったので、経験則だけで説明します。バッファ組成を酸性にすると疎水性が高まり、逆にアルカリ性にすると疎水性が低下します。
- この原理を利用して、クロマトグラフィのカラムのレジンの洗浄・再生処理には、強アルカリ性のバッファが使われます。
- 溶液の温度
- 反応論や溶解度の話になります。温度が高いと分子のブラウン運動が大きくなり、溶解度は一般的に高くなります。逆に、温度が低くなるとブラウン運動は低下し、溶解度は低くなります。すなわち、温度が低いほど沈澱になりやすいと推察されます。しかし、反応論的には、反応しずらくなるため、疏水性を利用する疏水クロマトにおいては、タンパク質のレジンに対する反応としての吸着性は低下するため、低い温度での疎水クロマトはワークしなくなります。
- 溶液の初期の塩濃度
- 塩析させる場合、塩濃度を高めるので、単純に初期の濃度を問題にしているだけです。
- 無機塩の種類と濃度
- 塩析させやすい塩が知られています。硫酸アンモニウムがそれです。でも、疏水クロマトにはあまり相性が良くありません。そこで、もっとマイルドなNaClや、クエン酸(Na)などが使われます。
塩を添加する方法による沈殿化の手法は、タンパクの精製に適するレジン(樹脂)がなかった昔に多用された技術です。この技術にはデメリットもあります。沈殿化したタンパク質は、沈澱を作る過程から状態を維持する過程で、タンパク質変性のリスクが高まります。理由は、沈殿化により、必要以上に強固に寄り集まったタンパク質が、水溶液に戻すときに再溶解しない場合がある事です。再溶解時に溶解しやすいようにする添加剤としての補助的に働くものがあります。グリシンなどのアミノ酸などは、その一種と考えられます。
タンパク質の沈殿化法による精製手法の代替法が存在します。以下の課題について解決し得る方法です。それは、疏水クロマトグラフィー(HIC)です。ここでは、HICについては論じていません(はりきり)。
沈殿化法の課題
- 沈殿化したタンパク質には,条件によっては再溶解の困難性というリスクがあること.
- いれまでは,工業的に遠心機は使用しにくかったが,最近では連続遠心と自動的に沈殿画分を回収できる機種も開発されている
ホフマイスター系列
1888年からのHofmeisterらの色々な塩を使った塩析実験から得られた塩析の強さは、ホフマイスター系列と呼ばれます。塩析効果の高い塩は利尿作用があり、逆溶解させる塩は下痢作用があると記述があります。
タンパク質の凝集剤としての塩・有機溶媒・高分子 (2015), 生物工学, 第93巻
https://www.sbj.or.jp/wp-content/uploads/file/sbj/9305/9305_tokushu_1.pdf
デバイ – ヒュッケル理論
静電相互素作用が主たる原理であるとするとデバイーヒュッケル理論で説明できる。しかし、実際には、タンパク質の塩析曲線はベルシェイプを示し、塩の種類によって異なる曲線を示すとの報告(1932年のGreenら)がある。すなわち、静電相互作用だけでは説明がつかず、別の相互作用や水の構造変化が影響していとる予想されていた。
イオンは水の水素結合ネットワーク
しかし、イオンは水の水素結合結合ネットワークに影響を与えないという論文が報告(2003)され、溶液中の水の構造を変えるのではなく、タンパク質の表面にある水和水に影響して、タンパク質の性質に影響しているのであろうと考えられた。
その理屈は、コスモトロープが水和水の秩序化→表面張力の増加→溶液は表面を減らす→タンパク質が凝集する。この理論は、リゾチームの凝集速度と溶液の表面張力の間に、正の相関があるとの結果と矛盾しない。
塩の種類により水和水の量に変化を生じさせていることについては、選択的相互作用の量として定義すると、
選択的相互作用の量 =塩(溶質)がタンパク質に結合している量 − 水和水により脱離してしまつた溶質の量、と定義する。値が正であれば、結合している溶質の量の方が多い、負であれば、結合している水和水の量の方が多い。
硫化物イオンの選択的相互相互作用の量は、塩化物イオンより小さい値を示すし、硫化物イオンは、塩化物イオンと並べて、タンパク質表面から選択的に排除されていることになる。
ホフマイスター系列
塩析する能力を示す。
塩析しやすい (コスモトロープ) > CO3 > SO4 > H2PO4 > F > Cl > I > SCN > NH4 > K > Na > Li > Ca > Mg > 溶解 (カオトロープ)
ホフマイスター系列は、周期表との規則性が見られる。
ハロゲン属では、 周期表順に同じく、
塩析しやすい > F > Cl > Br > I > 溶解
である。
アルカリ金属のカチオンでは、前述の逆となっている。したがって、沈殿材傾向は、イオンの半径や電子密度、質量で説明できることを示唆している。ただし、硫酸イオンやグアニジウムイオンなど複雑なイオンとは別の説明が必要と考えられる。
タンパク質の溶解度
一般的に、タンパク質の溶解度は、イオン濃度を増加させると増加し、それは極大値があり、ベルシェイプを示す。
デバイーヒュッケルの理論
デバイーヒュッケル理論で説明すると、塩を添加していくと、溶解から凝集まで一直線に状態変化する。低濃度では、静電遮蔽によってタンパク質の分子間の反発力が静電遮蔽により弱まる→分子の容積が減る→溶解度が増す、と説明できる。更に塩を加えていくと、タンパク質間のファンデンワールス力や疎水性相互作用などの引力が強まる→凝集する、と説明できる。しかし、実際には、溶解→凝集→溶解なるため矛盾がある。
コスモトロープ
コスモトロープ; kosmotropeは,水の水素結合ネットワークを秩序化(コスモス)する。Structure Makerとも呼ぶ.
タンパク質表面の水和水について考えてみると、溶解状態のタンパク質液が、凝集するまでのイベントは、以下の様になる。
「秩序化」→「気液界面の表面張力を増加させる」→「広くなった界面は不安定になる」→「溶液は安定化させようとする」→「表面を枯らそうとする→タンパク質はより集まる」→「凝集する」
カオトロープ
カオトロープ; chaotropeは,水の水素結合ネットワークを無秩序化(カオス)する。溶解する理論すは、上述の逆の理屈である。Structure breakerとも呼ぶ.
水構造緩和に対するコスモトロープとカオトロープ塩の影響
https://bibgraph.hpcr.jp/abst/pubmed/33031702
表面張力
水和を理解するための指標の一つ。surface tension, 表面をできるだけ小さくしようする性質。