タグ: MODERNA
-
[Vaccine] 世界で開発された 新型コロナウイルス用ワクチンの有効性 – Pfizer, Moderna, Astrazeneca, Sinovac [2021/06/15]
Post Views: 1,099 はじめに 変異株は、イギリス株に加えインド株(デルタ株)が、感染力が良いた…
投稿者

-
[Vc] Moderna – COVID-19 ワクチン臨床(Phase 3の中間結果は94.5%の有効性を示した – ID19527 [2020/11/16]
Moderna社は、新型コロナウイルスのmRNAワクチンを開発している。臨床は、Phase 3を進めており、中…
投稿者

-
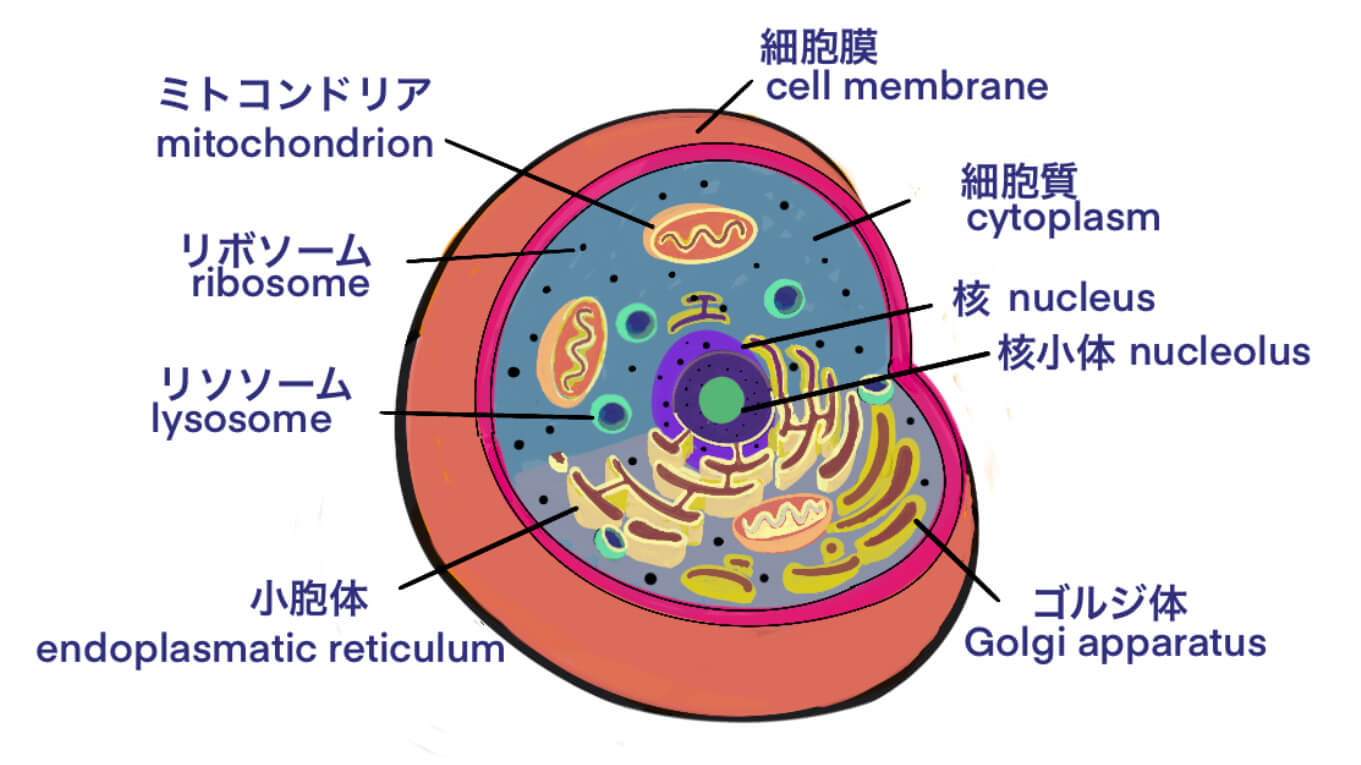
[Vc] mRNAワクチンの製造方法、moderna社とBiaseparations、その他から概略を学ぶ – ID15769 [2021/05/10]
moderna社のデモ・ビデオから、mRNAの開発初期の製造法、及RNAを製造委託する場合の受託会社とその製造…
投稿者

-
[Bio-Edu] mRNAワクチンの剤形 – LNP; Lipid Nano Particle – [2021/12/05]
Post Views: 1,264 ID15607 はじめに mRNAワクチンの細胞内への伝達としてLNP技術…
投稿者

-
[Vc] 核酸ワクチンとは DNAワクチンとmRNAワクチン – ベクターワクチンとの違い – ID15040 [2020/09/10]
Post Views: 1,001 ID15040 核酸ワクチン ワクチンの目的は、病原性の抑制に直接的/間接…
投稿者

-
気になる企業 – Moderna – 新モダリティ(mRNA)・ワクチン (新型コロナウイルス) で駆ける / Phase IIIの中間結果では94.5%の有効性を示す – LNP製剤による2~8℃保存が可能である優位性 – ID15029 [2020/12/03]
新型コロナウイルスのワクチン開発を進めている米国のバイオテクノロジー企業MODERNA社の開発の仕方から、その…
投稿者