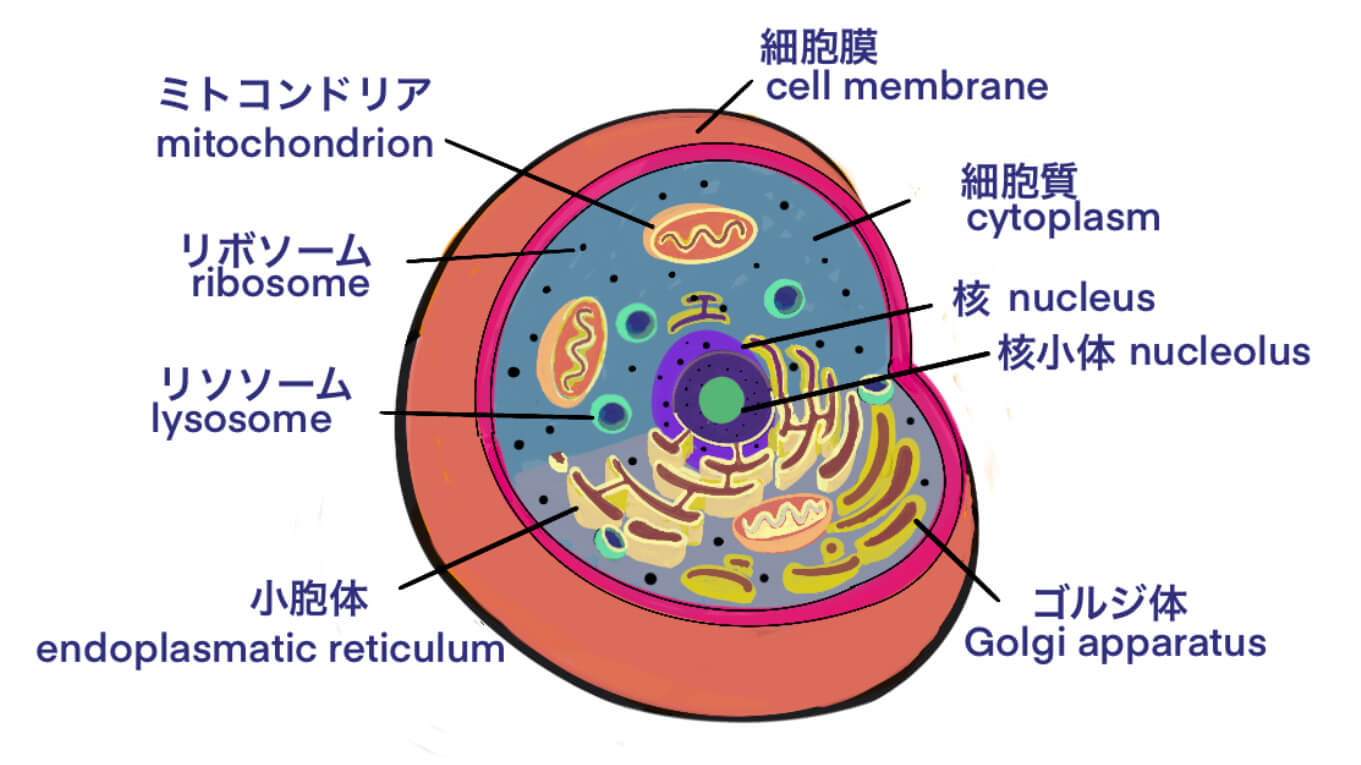
タグ: cell
-
[Bio-Culture] Poloxamer 188 (Pluronic F-68) – バイオリアクターの撹拌翼による細胞のダメージを抑制 [2021/02/24]
Post Views: 1,160 Poloxamer 188 Poloxamer 188という名称は、馴染み…
投稿者

-
[Bio-Vector] 人工染色体 – 目的細胞に導入して安定発現細胞株を作る – AAVベクターの生産株として適用できるのか? – chromocenter/TaKaRa [2021/01/15]
Post Views: 1,028 はじめに 遺伝子組換えで目的物を作る方法には、一過性発現と安定発現細胞株を…
投稿者

-
[Bio-Education] 細胞のモノクローナル化のための基本原理 – 最新装置を中心に解説 – [2020/09/03]
Post Views: 962 ID22024 細胞のモノクローナル化のための3つの基本操作 細胞をモノクロー…
投稿者

-
[用語] Transfection ; トランスフェクション – 遺伝子を細胞内に入れる
Post Views: 961 transfection transfection ; トランスフェクションは…
投稿者