カテゴリー: BIOLOGICS
-
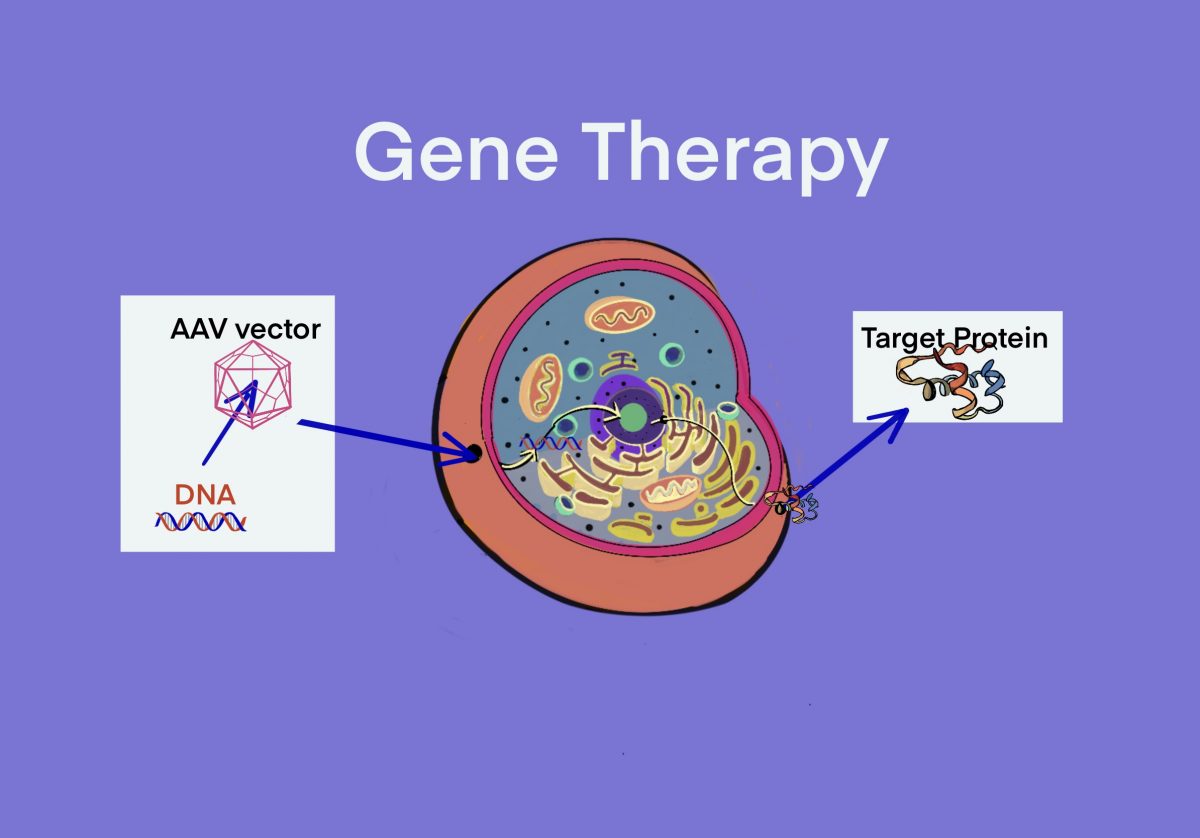
[遺伝子治療] アデノ随伴ウイルス(AAV)ベクターによる遺伝子治療薬 – 学者の承認済み/間近/臨床試験中 – ID1124 [2020/07/17]
Post Views: 445 AAVベクターによる遺伝子治療 2020/7現在、承認及び間近の品目 Zolg…
投稿者

-
[Bio-Edu] IgGの精製はProtein Aに対する親和性を利用する – 溶出バッファは何を使う? – ID7074 [2021/02/04]
Post Views: 704 IgGの精製 IgGという蛋白質は、Protein Aという蛋白質に対して強い…
投稿者

-
[Bio-Edu] RNA とは – mRNAはタンパク質を作る直接的な設計図 – その他 rRNA, tRNA – ID7254 [2020/01/15]
Post Views: 594 主なRNAは3種類 mRNA: messenger RNA rRNA: rib…
投稿者

-
[Bio-Edu] 遺伝子 – 生体内におけるDNAからタンパク質の合成 ・基礎知識 – [2020/06/13]
Post Views: 630 ID2216 遺伝子 遺伝子組換え技術を知るには、遺伝子の知識が必要だ。基礎知…
投稿者

-
[Kw] 人や動物において社会性の回復に「IL-17」と「IFN-γ」が関わっている
Post Views: 556 知恵熱 という言葉をききたことがあるだとうか。僕らの世代では、小さい頃に急に高…
投稿者

-
気になる企業 – Acepodia – ID6990 [2020/01/12]
Post Views: 594 Acepodia Cell Therapyをメインにするプライベートのバイオベ…
投稿者

-
[ED] 生物学 (レジメ) – 生物学とその方法、生命の科学的基礎、生物多様性を整理する – ID6988 [2020/11/03]
Post Views: 571 生物学 東京医科歯科大学のサイトに掲載の資料をレジメとしてまとめた。 ベテラン…
投稿者

-
[Bio-Culture] CHO細胞の培養における制御パラメータ、添加物及び装置・設備の事例 – ID6721[2020/09/08]
Post Views: 1,122 細胞培養とは 細胞を無菌・人工的に育てること 制御パラメータ 培養装置 細…
投稿者

-
[Bio-Edu] バイオ医薬品における生産細胞株の構築の方法 – ID5029 △[2020/08/19]
Post Views: 750 細胞株の構築 最近のバイオ医薬品の生産細胞株構築フローを以下に示します。 Ho…
投稿者