タグ: purification
-
[rAAV-DSP] AVB Sepharose High Performance – ID2292 [2019/09/21]
Post Views: 488 AVB Sepharoseの概要 吸着可能なAAVの血清型 Resinの特性 …
投稿者

-
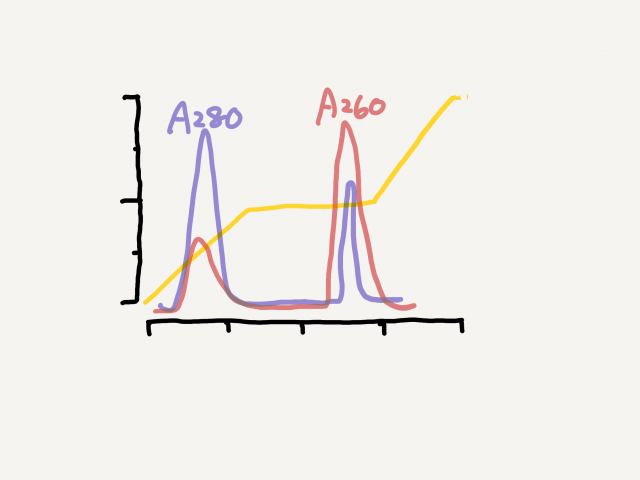
[rAAV-Edu] POROS CaptureSelect (AAV精製 resin) の性能とAEXによるfull/emptyの分離 – ID2271 [2019/09/18]
Post Views: 503 AAVX Resinの特徴 複数の血清型AAVを吸着 POROSは、Therm…
投稿者

-
[rAAV] rAAVベクターの精製方法 – Universal Method (2018) – ID2266 [2019/09/18]
Post Views: 509 はじめに 遺伝子治療薬のデリバリー・システムとしてAAV使用が盛んです。今後は…
投稿者

-
[Data Link] Purification of rAAV-1 and -9 with ultracentrifugation-free technique towards GMP production.(2013-2015, 科研費研究) – ID2225 [2019/09/15]
Post Views: 438 Purification of rAAV-1 and -9 with ultr…
投稿者

-
[Bio-Edu] 血漿由来の抗体精製 – Poll AcroSep resin), 2009 – ID14 [2019/08/12]
Post Views: 438 血漿中の抗体(IgG)を精製する方法 2019年現在、抗体医薬品のほとんどは、…
投稿者

-
[Bio-Lab] GE Healthcare PD-10 Column – カスタムな使い方として、中身を取り除いて、好みのレジンを詰める方法 – ID776 [2021/03/10]
Post Views: 677 PD-10カラム 脱塩カラム 平衡化バッファで平衡化 ~1mLをロードして、平…
投稿者

-
[Data Link] rAAV vectorの沈殿法を使った精製方法に関する文献のリンク – ID745
Post Views: 375 文献情報のみ A simplified purification method…
投稿者

-
[Bio-Edu] タンパク質(蛋白質)の精製 – 基礎編 – 不純物の定義、RefoldingからUF膜精製、タンパク質精製の定石まで – そしてタンパク質を知る – ID686 △[2021/06/03]
タンパク質精製に関する温故知新、誰でもできるタンパク質の精製概要が理解できる基礎編を解説。最近のrAAV精製を…
投稿者