タグ: codon
-
[Vc] mRNAワクチンとは – Sanofi, Modernaなどが開発を進めている – ID15091 [2020/05/23]
mRNAを用いた医薬品は、新型コロナウイルスに対するワクチンとして、開発完了が近々見込まれている。mRNAワク…
投稿者

-
[用語] codon ; コドン – 遺伝子の構成要素はA,T,G,C、アミノ酸は3つの組み合わせ
Post Views: 613 codon コドン(英: codon)とは、核酸の塩基配列が、タンパ…
投稿者

-
[Bio-Edu] RNA とは – mRNAはタンパク質を作る直接的な設計図 – その他 rRNA, tRNA – ID7254 [2020/01/15]
Post Views: 597 主なRNAは3種類 mRNA: messenger RNA rRNA: rib…
投稿者

-
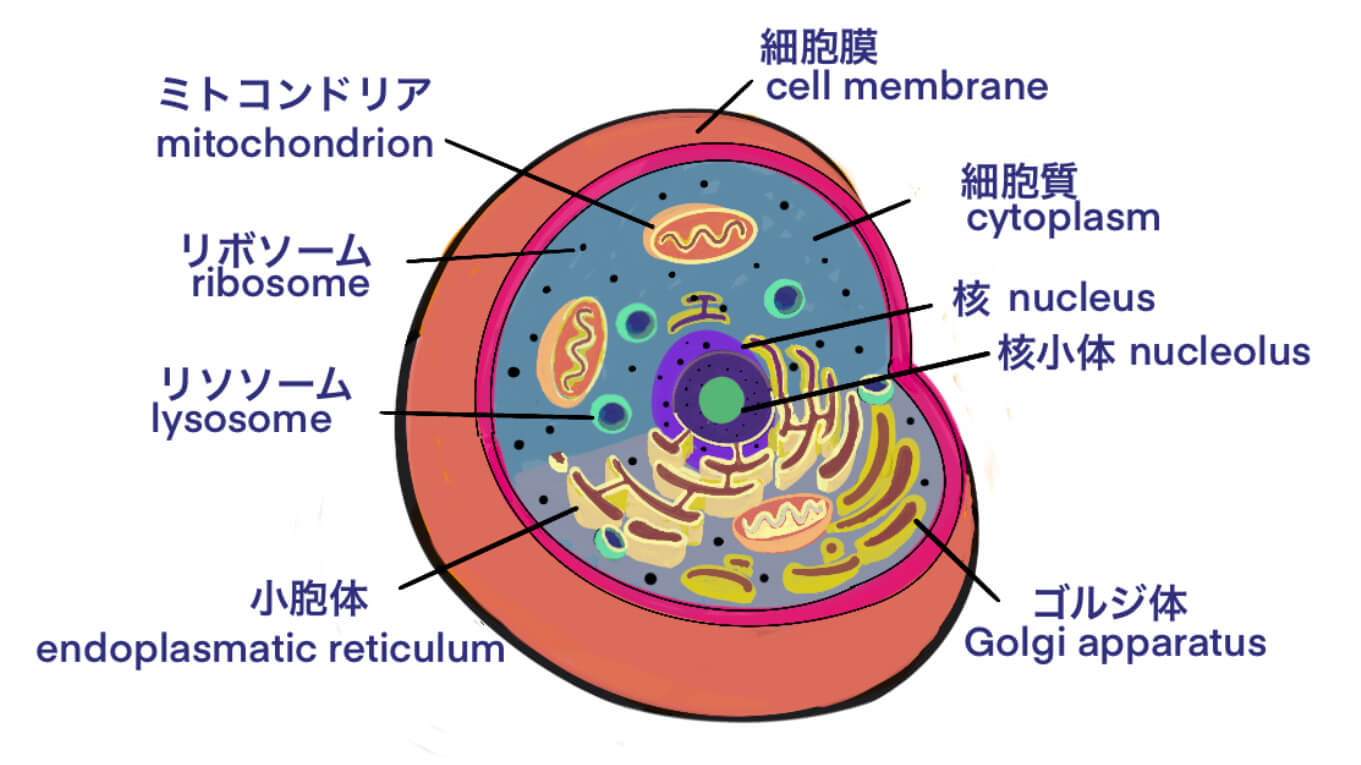
[Bio-Edu] 遺伝子 – 生体内におけるDNAからタンパク質の合成 ・基礎知識 – [2020/06/13]
Post Views: 635 ID2216 遺伝子 遺伝子組換え技術を知るには、遺伝子の知識が必要だ。基礎知…
投稿者

-
[健康] 神経疾患(ミオパシー、てんかん)に共通する異常なリピート配列の発見 – リピート配列は開始コドンがなくてもたんぱく翻訳される – ID1093 [2020/07/11]
Post Views: 371 はじめに 2019/07, 東大、3つの神経筋疾患に共通する異常なリピート配列…
投稿者