タグ: gene-therapy
-
[Gene Therapy] Valrox – 血友病Aの遺伝子治療法薬として世界で初めて市販なるか – 200~300万ドルを予定 [2020/06/22]
Post Views: 974 ID23142 Valrox Valroxは、アメリカのBIOMARIN社が開…
投稿者

-
[Bio-Edu] Plasmid – バイオロジクスには欠かせない遺伝子組換え技術、そして rAAVを作るまで! – AAV Vector配列の例 [2020/08/05]
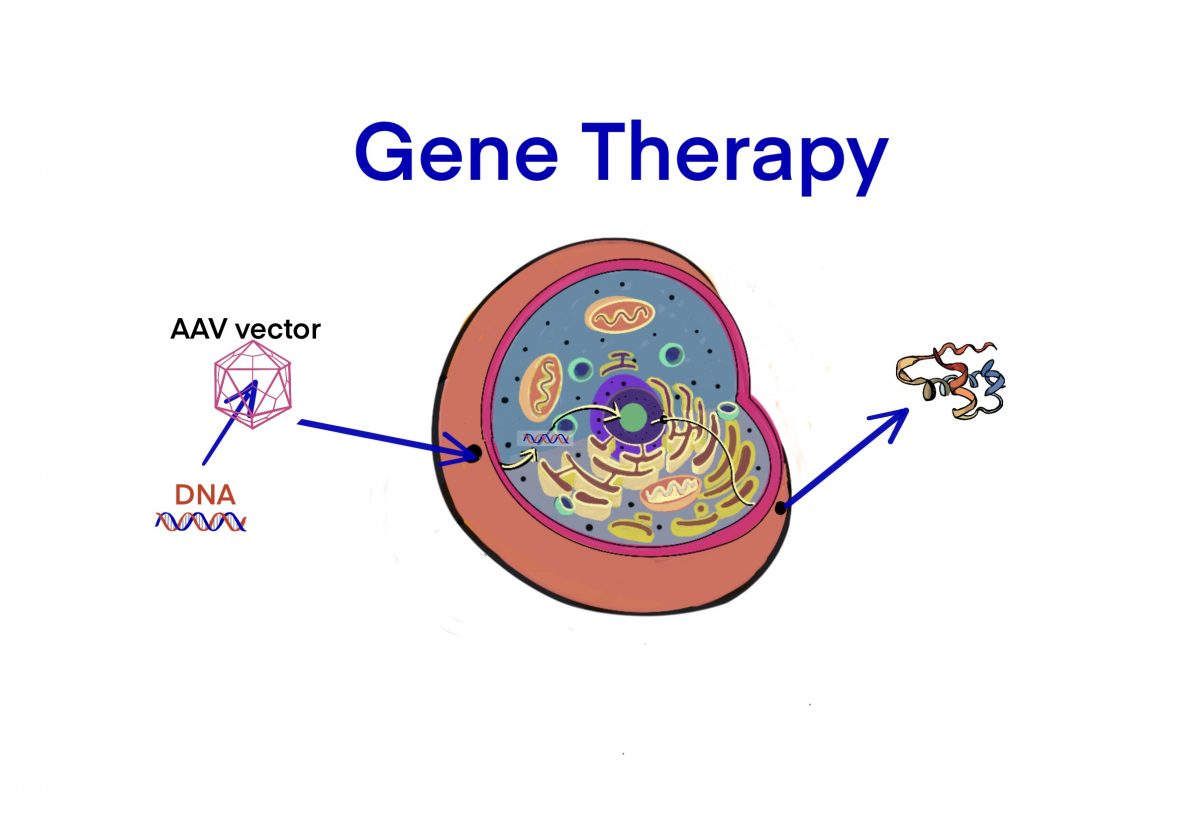
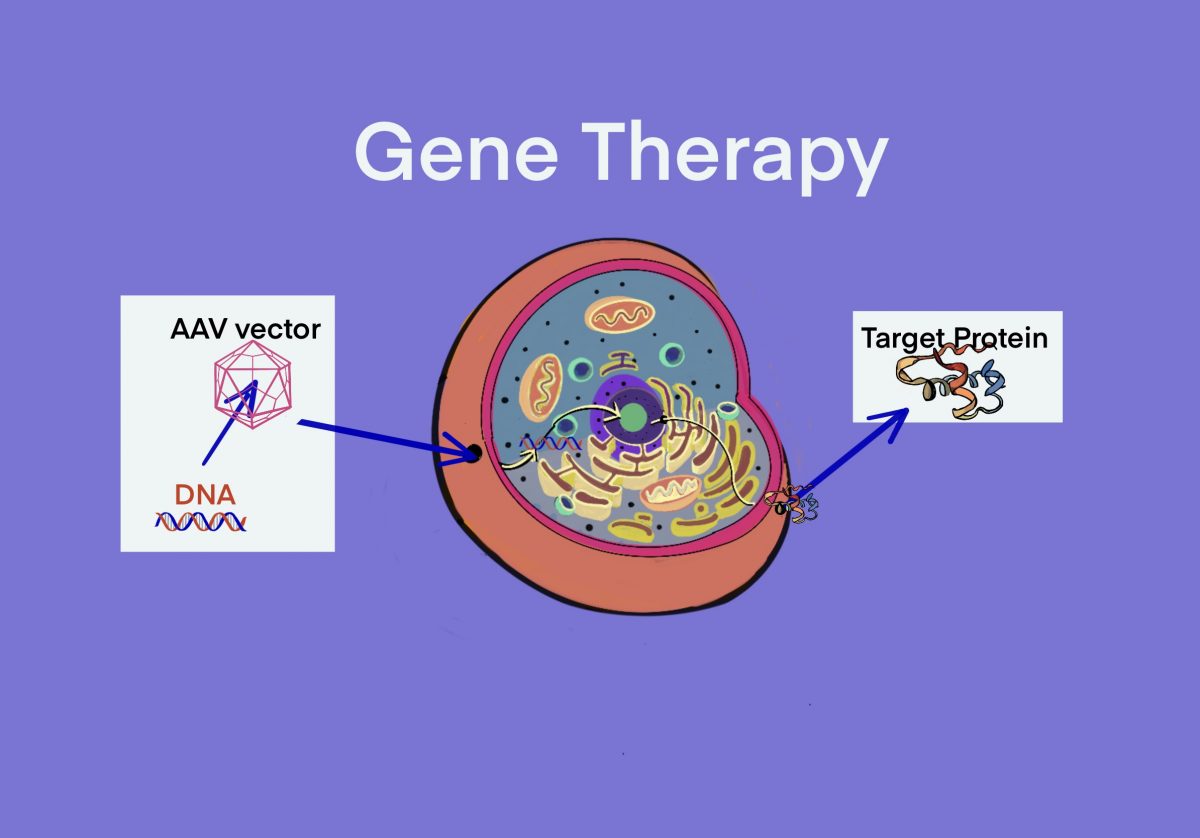
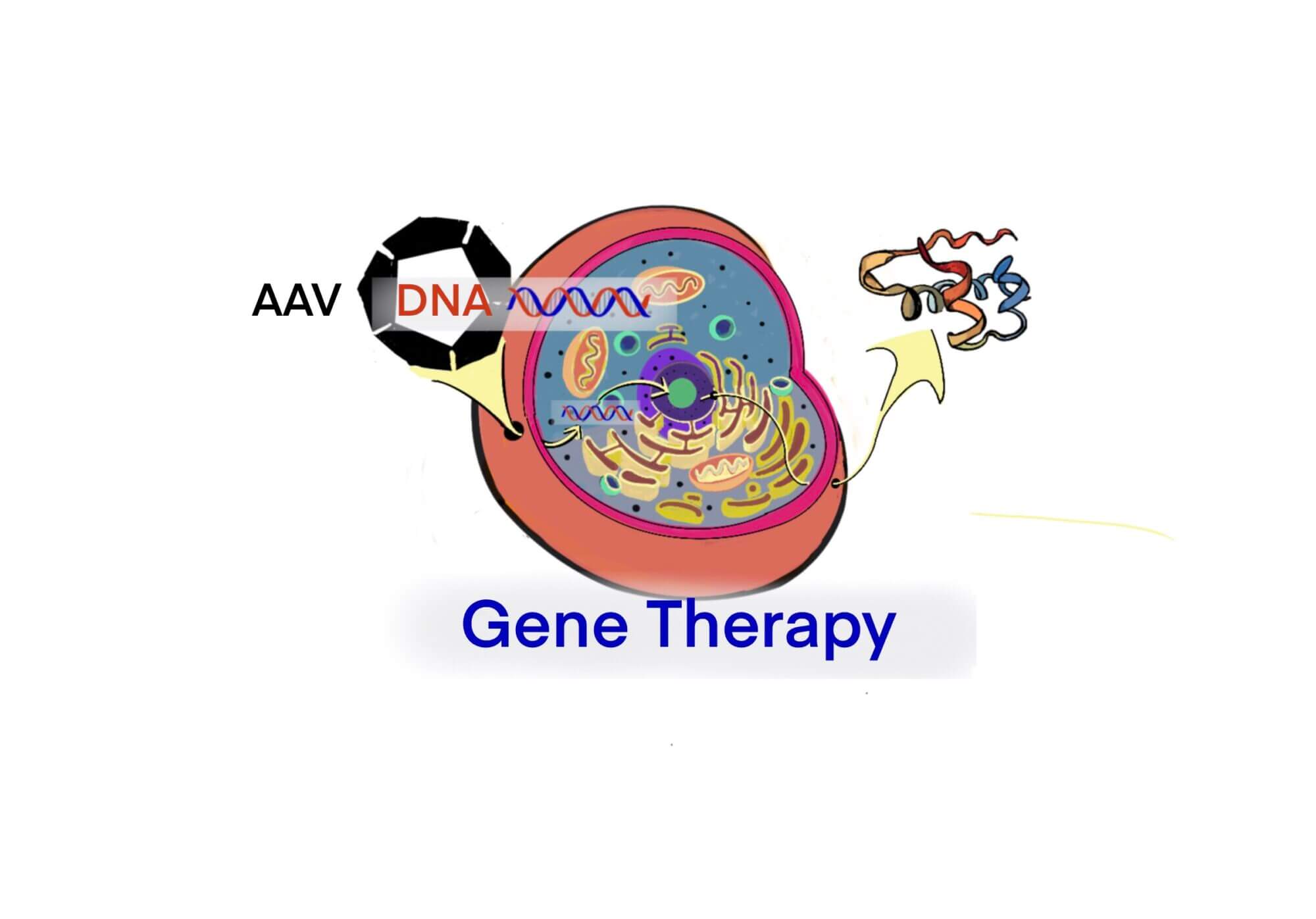
rAAVによる遺伝子治療薬の開発には、遺伝子組換え技術が使われている為、この知識がなくてはならい。 rAAVを…
投稿者

-
[Bio-Edu] ウイルスベクターの比較 – AAV – Adenovirus – Lentivirus – by Vigene Biosciences社 [2020/6/15]
Post Views: 875 Vigene Biosciences Vigene Biosciencesは、…
投稿者

-
気になる企業 – WuXi Advanced Therapies – 遺伝子治療CDMO [2020/06/15]
WuXiグループは、抗体医薬に続き遺伝子治療においても、バイオロジクスのCDMOとして投資に余念がない
投稿者

-
気になる企業 – AVIGEN – Genezymeに買収 – △ID11266 [2020/03/03]
Post Views: 688 現在は、Avigen社は存在しない。 「気になる企業」シリーズ。バイオ医薬品に…
投稿者

-
[ゲノム編集] デュアルAAVデリバリーシステムによるマウスのデュシェンヌ型筋ジストロフィーの治療研究 (CRISPR-Cas9を補助する) – ID9877 [2020/08/22]
ジュジェンヌ型筋ジストロフィーの治療薬の研究として、AAVを活用したゲノム編集型遺伝子治療研究の文献を概説し、…
投稿者

-
[遺伝子治療] アデノ随伴ウイルス(AAV)ベクターによる遺伝子治療薬 – 学者の承認済み/間近/臨床試験中 – ID1124 [2020/07/17]
Post Views: 449 AAVベクターによる遺伝子治療 2020/7現在、承認及び間近の品目 Zolg…
投稿者

-
[GT] 遺伝子治療の課題 – H30, 経済産業省より – ID2031 [2020/01/08]
Post Views: 379 2019現在における遺伝子治療薬の製造課題 Full particleとEmp…
投稿者

-
気になる企業 – Audentes Therapeutics – アステラス・グループ – ID4488 [2020/07/08]
Post Views: 573 Audentes アステラス製薬グループ (2019/12) Audentes…
投稿者

-
[Bio-rAAV] 遺伝⼦治療における代表的な委託製造会社 (CMO) – ID1881 [2021/02/08]
Post Views: 477 rAAV vectorを製造するCMOリスト 企業サイト サイト 製造サイト …
投稿者