タグ: MolMed
-
気になる企業 – Molecular Medicine ;MolMed – [2020/11/09]
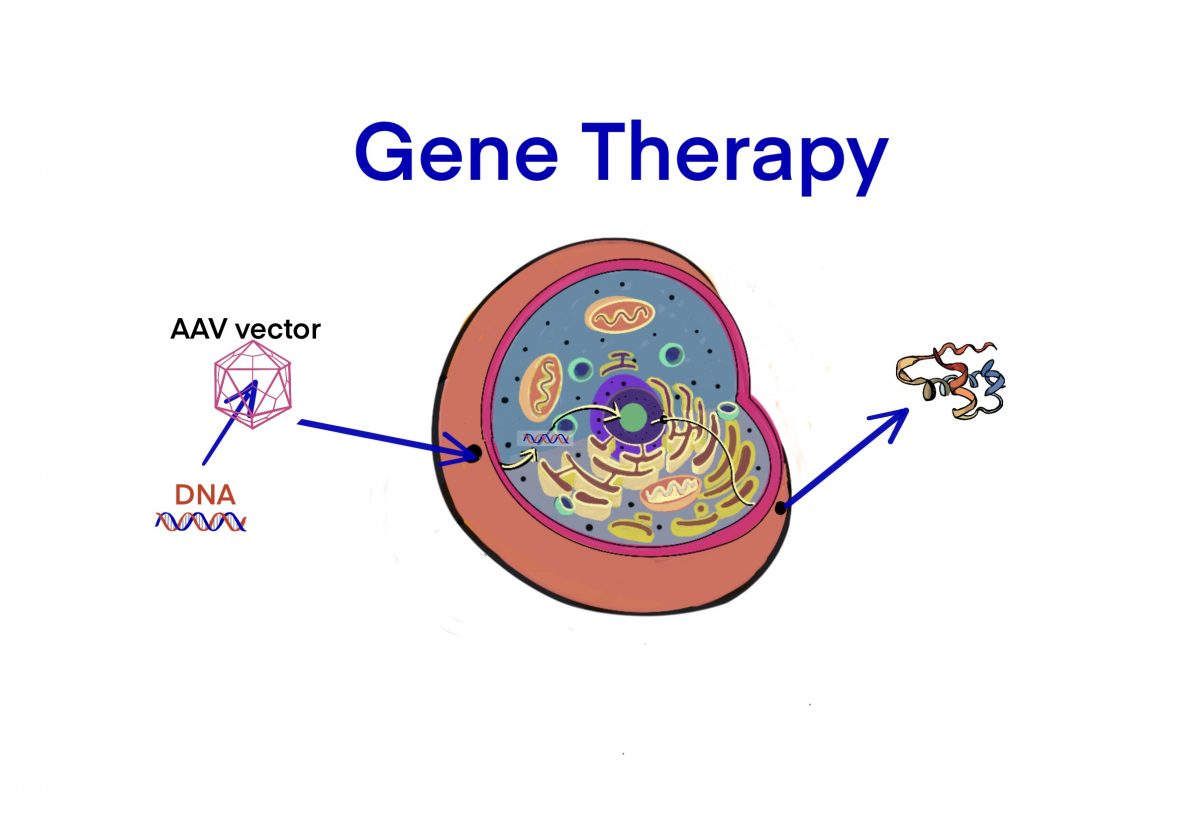
Post Views: 779 ID12516 MolMed イタリア ウイルス・ベクターを用いた遺伝子治療薬…
投稿者

-
[GT] 承認された遺伝子治療薬 – まとめ – ID10658 [2020/06/09]
Post Views: 784 まとめ 2020年3月現在、承認された遺伝子治療薬の数は、一桁であるが、既に世…
投稿者

Post Views: 779 ID12516 MolMed イタリア ウイルス・ベクターを用いた遺伝子治療薬…
投稿者

Post Views: 784 まとめ 2020年3月現在、承認された遺伝子治療薬の数は、一桁であるが、既に世…
投稿者