タグ: Genome Editing
-
気になる企業 – Oxgene™️ (Oxford Genetics LTD) – LentivirusのPCL/rAAV高生産できるHEK293細胞株/PCLの構築手順 – ID12556 [2020/11/22]
Post Views: 826 Oxgene™️ Oxgene™️ by Oxford Genetics LT…
投稿者

-
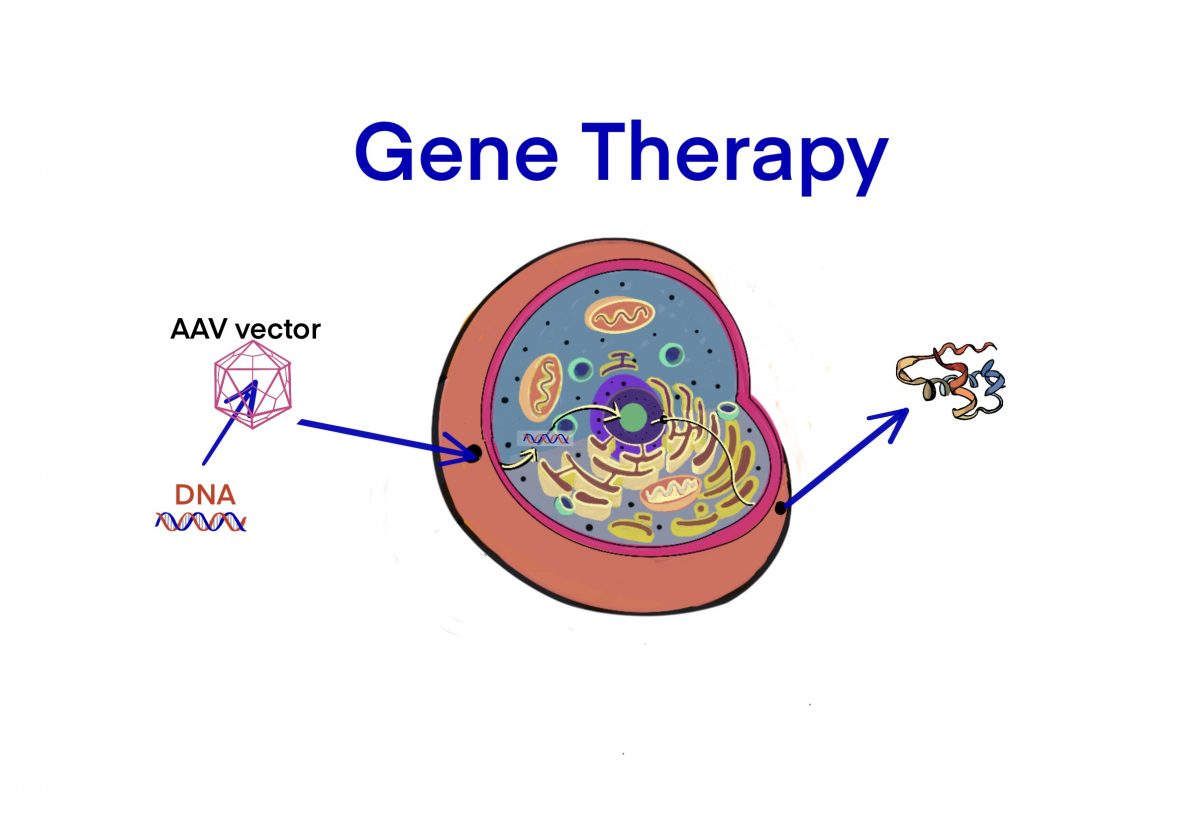
[ゲノム編集] デュアルAAVデリバリーシステムによるマウスのデュシェンヌ型筋ジストロフィーの治療研究 (CRISPR-Cas9を補助する) – ID9877 [2020/08/22]
ジュジェンヌ型筋ジストロフィーの治療薬の研究として、AAVを活用したゲノム編集型遺伝子治療研究の文献を概説し、…
投稿者

-
[Bio-Edu] ゲノム編集/CRISPR-Cas9 [2023/10/20]
Post Views: 397 CRISPR CRISPRは,clustered regularly inte…
投稿者