タグ: 培養
-
[rAAV-Production] – 治療用AAV Vector製造 – 考慮事項 – SM-ID12844 [2020/10/14]
Post Views: 940 ウイルス・ベクターと宿主細胞の準備 目標のAAVベタクー発現量 15cm ディ…
投稿者

-
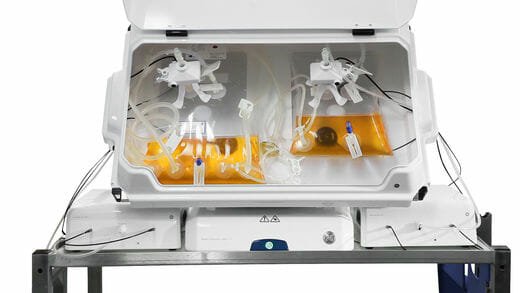
[Bio-Equip] WAVE 25 Rocker – GE – ID11509 [2020/03/06]
Post Views: 751 WAVE 25 Rocker ロッキング型のバイオリアクター。25Lまで培養可…
投稿者

-
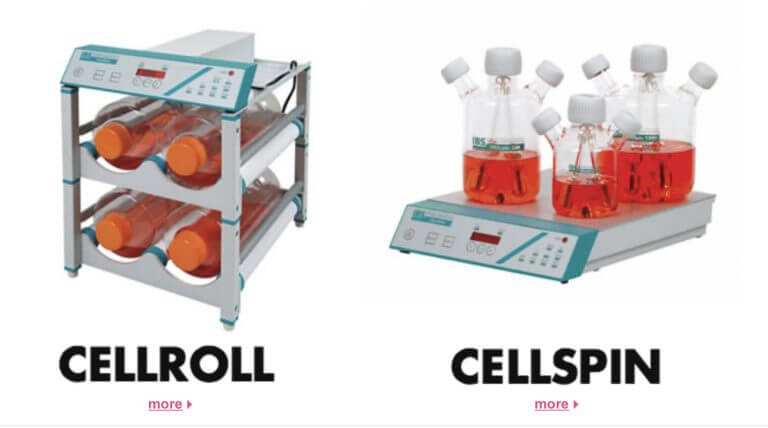
[Bio-Process] 拡大培養/Subculture – ID9342 [2020/02/01]
Post Views: 715 拡大培養に使用する機器、装置 WAVE BIOREACTOR Waveシリーズ…
投稿者

-
[Bio-Process] 細胞の凍結融解から拡大培養の開始 – フラスコ培養/Inoculum – △ID9636 [2020/02/01]
Post Views: 746 Bio-Process-Inoculum 凍結保管セルバンクの融解とフラスコ培…
投稿者

-
[Bio-Edu] 遺伝子組換え大腸菌からタンパク質を精製する製造フロー概略 – ID6624 [2020/01/09]
Post Views: 651 製造方法の概要 大腸菌に目的蛋白質の遺伝子を導入 大腸菌の培養 刺激剤(IPT…
投稿者