CDC; Centers for Disease Control and Prevention; アメリカ疾病予防センター、ジョージア州アトランタ
ブログ
-
![[WordPress] その昔憧れた、パーソナル・データベース生活を実現。 – イベント・プラグイン – を選定/導入する [2020/05/23]](data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAAwAAAAD3AQAAAACChQ4fAAAAAnRSTlMAAHaTzTgAAAAuSURBVHja7cEBDQAAAMKg909tDwcUAAAAAAAAAAAAAAAAAAAAAAAAAAAAAMC1AV2XAAHCKzNSAAAAAElFTkSuQmCC)
[WordPress] その昔憧れた、パーソナル・データベース生活を実現。 – イベント・プラグイン – を選定/導入する [2020/05/23]
ID18377
イベント・プラグインの使用目的
背景
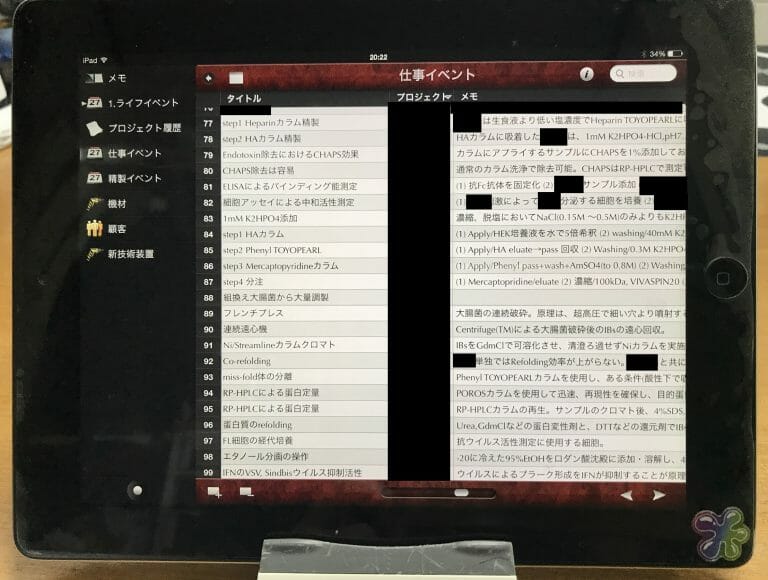
初代iPadが発売されてから、iPad3くらいまでは、iPad用のDatabaseアプリが沢山ありました。
使い方としては、データベースとして残しておきたい情報や自分のイベントなどについて、その情報のデザインを自分で行い、そのフォーマットにデータをエントリーしていくものです。
以前にエントリーしたデータを見たくなった時、そのデータは検索により瞬時に得ることができます。しかも、端末がiPadやiPhoneなので、何時でも情報にアクセスできるという憧れのデーターベース生活を達成できるアプリたちでした。
編集履歴
2020/05/23 はりきり(Mr)

中でも、デザインも機能も使いやすさも優れていたのが、Mac用のデータベースソフトで知られていたFileMaker (会社名も同じ)が開発した、iPad/iPhone用の
bento
でした(2012/07/16)。
更に、機能を求めるなら、FileMakeを購入してWindows/Macにインストールし、少しフォーマットを開発すれば、以下のことが可能となる予定でした。
- 親データベース自体は、Mac/Windowsに置く
- 端末であるiPad/iPhoneの「bento」から吸い出して外出
- オフライでのデータベースのアップデートや検察
- その後帰ってから、親データベースに「bento」で接続してアップデート
Windows用のFileMakerの購入も考えていましたが、2013年に突然の提供の終了となりました。
FileMaker、パーソナルデータベース「Bento」の提供を終了へ – ITmedia NEWS 2013/08/01 – より
あれから7年が経ちました(2020年)。1.5年前には、WordPressなるものがあることを知りました。WordPressには、mySQLのサブセットであるMaria SQLが搭載されていることも知りました。
目的
その昔憧れた、「パーソナルデータベース生活」は、今日、可能になった!! のではないでしょうか。
今回は、導入編です。
イベント・プラグインを選ぶ理由
WordPressのポスト機能を使用せず、イベント・プラグインを導入する理由ですが、やはり使い勝手の問題です。
- プライベートを維持できるか
- データー・エントリーは簡便か
- 複数のイベント表示は、タイトな表示が可能か、カスタマ泉性は高いか
検討したイベント・プラグイン
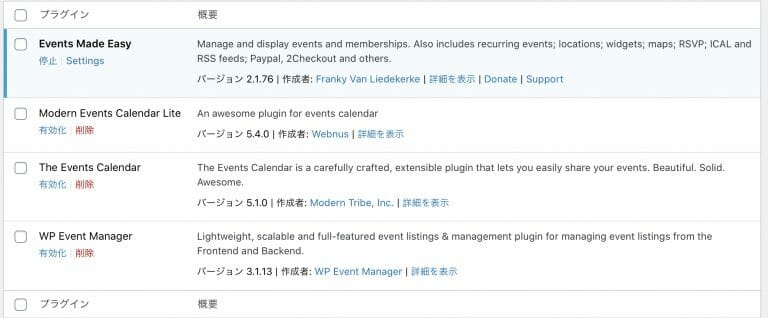
4つのイベント・プラグインを選択し、インストールしました。「Setting」を一通り確認した後、イベントのエントリーの具合を以下の内容で確認しました。
- イベント・プラグインを「event」で検索
- 目ぼしいプラグインの詳細に飛び、「スクリーンショット」を確認して、自分が望む表示なのかを確認
- 気に入ったプラグインは、「インストール」
- 結果的に、4つをインストールしました
- 各プラグインの「Setting/設定」を一通り流し読み
- イベントをエントリーしてみて、表示機能を探して表示さる
- 「Private」というキーワードが「Events Made Easy」プラグインにあることを確認
- フル機能が「Upgrage」しないといけいプラグインをボツにする
- 「Events Made Easy」はフル機能が提供されていることを確認
- 一通りのプラグインのエントリーのしやすさを比較
- 表示の比較

イベントプラグイン
Events Make Easy
を選択。
その結果、「Events Made Easy」を選定しました。更に、よりディープにつかいこんでみました。
- 30レコードほどのイベントを入力
- エントリーのしやすさの確認
- 一括管理のしやすさの確認
- 表示のショートコードの確認
- Widgetの確認
- Private機能の確認
選定理由
- フル機能が提供されている
- 色々な機能が装備されていおり、支払い情報関連、メーリングリスト関連、メンバーシップ関連など多数あり、現状は必要ないが、将来性を買った
- その内、有料版になると予想されるくらい完成度が高い
- エントリーが簡便にできる
- 表示など、ショートコードが充実しており、望む表示とカスタマイズ性も高く、将来的には使い込んでみたいと思った
- Widgetも使用可能
- イベントに「Private」を簡単に設定できる
- イベントに「カテゴリー」をセットできる
- WordPress内の検索機能ではヒットしないように、専用の検索を行うようになっている。
使い方
メニュー
最小限の設定と最小限のエントリーの概要
設定項目がおおいのですが、早速使ってみるための最小限の取り扱いについて、以下にまとめました。
- 多数の設定項目はあるが、ほとんど、デフォルトで良い
- 最小限のエントリーは、「タイトル」と「日付」を入力して保存する。その他、ロケーションなども使用可能
- カレンダーの表示には、固定ページを設定する
- カレンダーのWidgetも設定しておく
- 「Private」にセットしている場合、ログイン・ユーザーでなければ、カレンダーに表示されない。ログイン・ユーザーであれば、リンク付きで表示される
- 1点注意として、WordPress標準の検索では、引っかからない(タイトルさえ引っかからない)。これは、「Private」の維持としては正解である。
- 因みに、メンバーシップを構築できるUltimate Memberプラグインでは、WordPressの標準の検索で、秘密の投稿でもタイトルはヒットしてしまう。
- では、Events Made Easyで検索したい時、どうするか? 充実したショートコードを使用する(と現在は理解している)。ショートコードのサンプルは多数が紹介されている
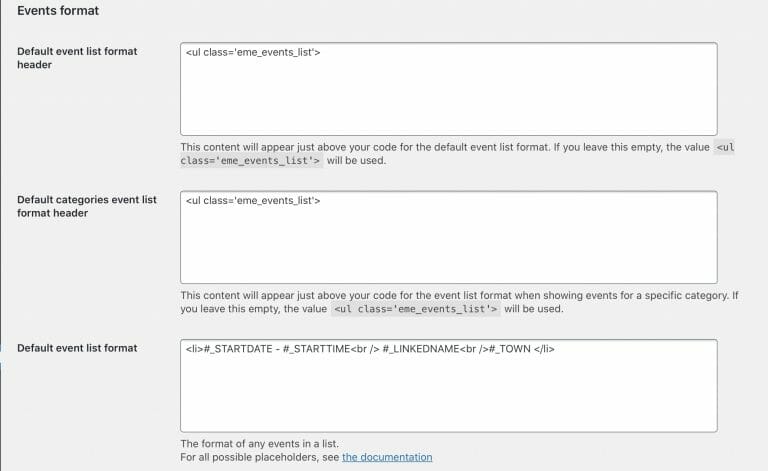
表示はどんな感じ?
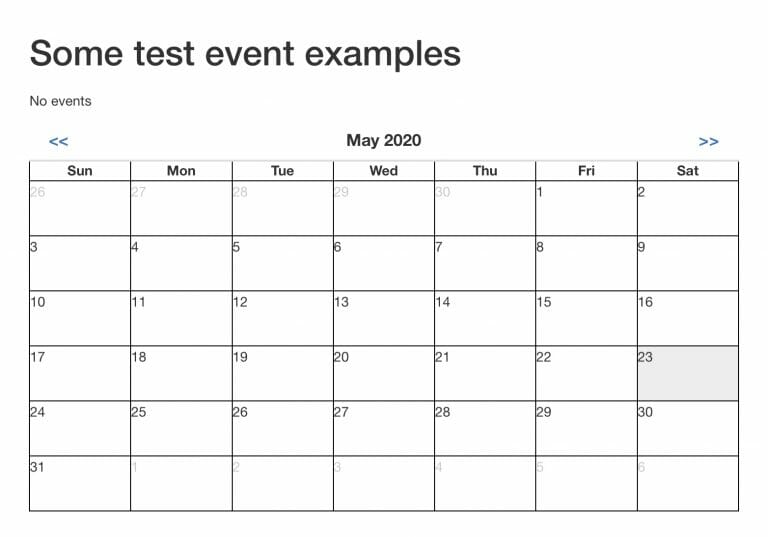
まだ、使い込んでいませんが、コンパクトにリスト化できれば、先ずは良しです。
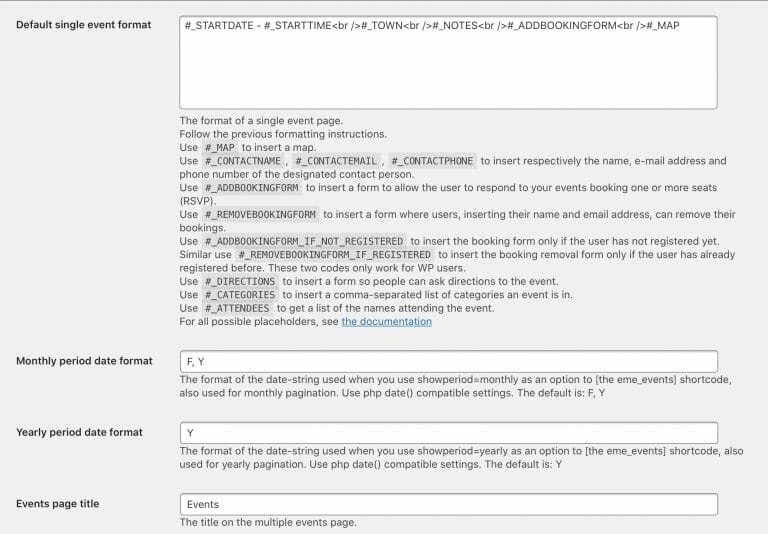
以下のショートコードで、1つのイベントのタイトル(リンク付き)が1行で表示されます。全体の俯瞰には、このシンプルさが最適です。
もちろん、日付のカラム内にリンク付きで「カレンダー」表示が可能です。これもシートコードの挿入で簡単に、PAGEに配置できます。ページの属性を非公開にすれば、そのカレンダーは、パーソナルなカレンダーになります。

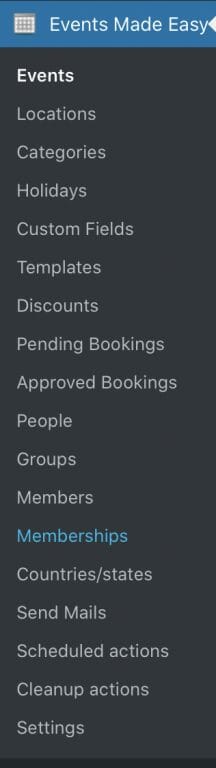
Events Made Easyのメニュー
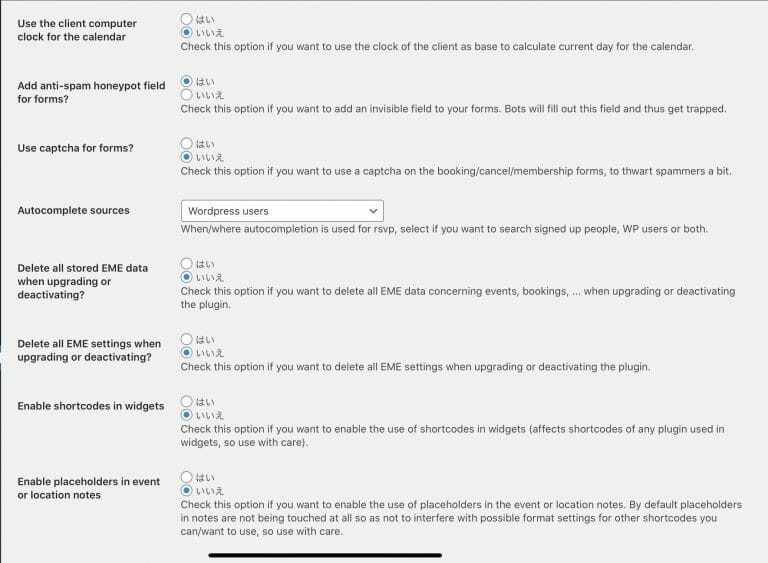
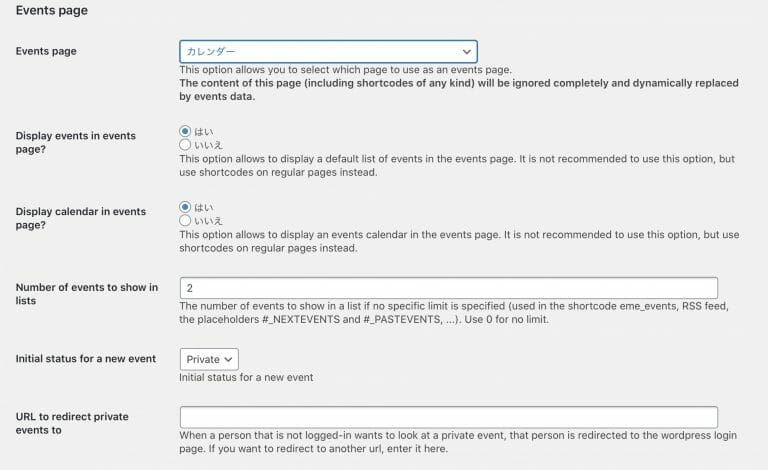
まだまだ、使いこなすには至っていないので、設定画面など写真のみで雰囲気を感じてください。今後、レポートしていきたいと思います。

Settingsのメニュー

Generalの設定


SEOの設定

Eventsの設定





Locationsの設定

以上
-
![[Bio-Edu] バイオ医薬品 (バイオロジクス)は、CHO細胞の技術革新と共に進展してきた [2020/08/05]](data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAB4AAAAU9AQAAAAA2EmbpAAAAAnRSTlMAAHaTzTgAAAFQSURBVHja7cEBDQAAAMKg909tDjegAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAA4M7qkAAXe1B3gAAAAASUVORK5CYII=)
[Bio-Edu] バイオ医薬品 (バイオロジクス)は、CHO細胞の技術革新と共に進展してきた [2020/08/05]
バイオ医薬品とは
バイオ医薬品は、英語でバイオロジクスと言います。バイオロジクスには、ヒトの体内に存在するタンパク性物質をターゲット(狭義)にしているため、よく知られている「抗体」以外のタンパク質も含まれます。
バイオロジクスは、当初、血漿分画製剤で知られているように血液から得られていましたが、技術革新により現在では、その目的物である医薬品は遺伝子組換えCHO細胞により得られるようになって久しく、正にバイオロジクスは、CHO細胞に関する技術革新とともに進展してきたと言えます。
以下、バイオロジクスについて、CHO細胞を使うアドバンテージをまとめました。ただし、CHO細胞が完全勝利ではありません。目的によっては、インスリン製剤など低分子量のタンパク質では、大腸菌が使用されています。
- 現在、バイオロジクスの代表は、「抗体」である
- その原材料は、
- 「血液、19世紀末・戦後 ~」、ジフテリアや破傷風などの感染症治療法として弱毒化毒素のウマへの投与によるマウ血清が感染症治療に高い効果があることがベーリング(behring)と北里柴三郎らにより明らかにされた
- 「B細胞のハイブリドーマ細胞化 (抗体に限る)、1975年~」、B細胞は、細胞ごとに単一の抗体を産生するが不死化させるためにミエローマ細胞を用いたハイブリドーマ技術が発展した。得られた抗体をmonolconal antibodyという。
- 「遺伝子組換え細胞」へと展開してきた
- source: Pharmacokinetics of Monoclonal Antibodies
- source : 抗体医薬とは, 熊谷泉 – 化学と教育 68巻 7号 (2020)
- 原材料として
- 「血液」
- 動物由来の場合では異種高原であることによる免疫原性の問題
- オリジナル機能のタンパク質を取得できる(血漿分画製剤)
- 量的制限
- ウイルス安全性に問題
- 「ハイブリドーマ」細胞
- 動物への抗原免疫(抗体作成)、脾臓(B細胞)とホスト細胞(ミエローマ)とのハイブリドーマ作製、など煩雑であり抗体に限定
- 動物への抗原免疫(抗体作成)、脾臓(B細胞)とホスト細胞(ミエローマ)とのハイブリドーマ作製、など煩雑であり抗体に限定
- 「遺伝子組換え技術」
- キメラ化 : 動物由来の可変領域とヒト抗体の定常領域を結合
- ヒト化抗体 : 動物由来のCDR (Complementarity Determining Region, VHとVLにそれぞれ3箇所ずつ存在)のみをヒト抗体に移植することで、約95%がヒト由来構造を維持
- 製造技術の進展による大量製造
- 実績としてのウイルス安全性(CHO細胞)
- 宿主細胞に関わる糖鎖(CHO細胞は実績として克服)
- 現在では様々な課題を克服できている
- 「血液」
- 遺伝子組換え技術での生産細胞
- 分子量が大きな抗体の産生細胞として、殆ど全てがCHO細胞が選択される
- 分子量が小さいインスリンやインターフェロンなどの産生細胞には微生物(大腸菌、酵母など)が使われる。
- CHO細胞
- バイオロジクス市販品で30年の実績
- ヒト型に近い糖鎖を付加でき、その他不純物に関する安全性の蓄積
- 立体構造を再現できる
- 高い培養生産性技術が蓄積(最大10g/L)
- 大腸菌
- 医薬品上の問題点
- 糖鎖を付加できないため糖タンパク質には不向き
- 高い産生量にするとInclusion body(不溶性)になる
- 立体構造をオリジナルに再現できない
- 対策
- 糖鎖問題は、目的タンパク質を限定
- 立体構造は、Refolding技術による正常化
- 医薬品上の問題点
- 酵母
- 1990年代に盛んな研究
- 医薬品上の問題点
- 糖鎖を付加できるが、ヒト型ではないため、抗原性の問題がある。
- 強力な蛋白分解酵素により目的タンパク質の分解問題
- 対策
- 糖鎖問題
- 目的タンパク質を限定する
- 糖鎖付加が無いタンパク質
- 糖鎖遺伝子のノックアウト
- 医薬品でない酵素など
- 分解問題
- 培養技術及ひ精製技術で対応
- プロテアーゼ遺伝子のノックアウト
- 糖鎖問題
CHO細胞・エニジニアリング
現在のバイオロジクス、特に抗体に関する遺伝子組み換え技術を使ったCHO細胞による生産性改善と取り組みは、以下の参考文献が概説として参考になります。
- 目的タンパク質の遺伝子組込み、得られる細胞の多様性(糖鎖修飾)
- 細胞株構築期間の長さ
- 得られた細胞株の培養最適化
- 比生産速度 pAB と 生細胞濃度 Xvの積分 = 生産濃度 P (IVC) (完全に理解できていません。今後要検証)
バイオ医薬品生産におけるプロダクションサイエンス (2013)
https://www.sbj.or.jp/wp-content/uploads/file/sbj/9109/9109_tokushu_3.pdf生産細胞の培養技術
産生株が高い生産能力があったとしても、その培養条件がマッチしていなければ高い生産性は達成できません。抗体医薬品の場合、投与される量が多いため培養生産性は課題の一つになります。
安定産生株の樹立と、その培養条件の開発の概説として、以下の文献が参考になります。
- 安定発現株
- 培養スケールアップ
- 培養プラットフォーム
- 電荷的多様性の制御
- 培養終了の判断
抗体医薬品生産培養技術の課題と展望 (2013)
https://www.sbj.or.jp/wp-content/uploads/file/sbj/9109/9109_tokushu_4.pdf抗体医薬品・Fc融合タンパク質
抗体医薬品について学ぶには、以下の項目を押さえておくことが重要です。「国立医薬品食品衛生研究所」のサイトに、「抗体」医薬品と「Fc融合タンパク質」について、まとめられたサイトがあります。
抗体医薬品について全体像を把握することができます。
抗体医薬品・Fc融合タンパク質
国立医薬品所品衛生研究所・生物薬品部
http://www.nihs.go.jp/dbcb/mabs.html抗体の分子的特徴として「Fc」と呼ばれる領域があります.Fcには抗原に対する結合機能は無く別の機能を持っていますが,抗原結合能を持っていないことから,この領域に,例えばPEGなどを結合させて,抗体自体の血中半減期を延ばしたり,がん抑制化学物質を結合させて,がん治療薬として機能を増強させたりと,このFc領域は利用されます.
https://bio.nikkeibp.co.jp/atcl/mag/btomail/17/12/19/00339/
バイオシミラーの基礎知識
バイオシミラーの基礎知識について、厚生労働省取材のセミナー資料があります。最近の情報であるためバイオロジクスに関しても最新情報を得ることができます。
バイオ医薬品とバイオシミラーの基礎知識 – 厚生労働省主催講習会「バイオ医薬品とバイオシミラーを正しく理解していただくために」- 2020年1月11日 (大阪科学技術センター 大ホール
https://www.mhlw.go.jp/content/10800000/000496079.pdf抗体医薬の品質について
日本における規制当局からのガイダンスがあります。
抗体医薬品の品質評価のためのガイダンス (2012)
https://www.pmda.go.jp/files/000206143.pdfCHO細胞以外の哺乳類細胞
バイオロジクスで使用される動物細胞は、CHO細胞が殆ど全てと述べましたが、用途によってはラッド由来の細胞の使用が試みられています。2020/6現在、日本で上市されているYB2/0由来抗体は、0、SP2/0は4つ、NS0は5つ、CHOは57つです。以下の課題は依然として残ります。
臨床段階で、YB2/0細胞由来の抗体医薬があります。YB2/0細胞は、フコース付加低減化が可能でADCC活性を高めることが可能な細胞株です。しかし、CHO細胞を代表する動物細胞の実績は、YB2/0細胞にはありません。YB2/0細胞は、2020/6現在、臨床試験が1社によって走っているのみです。新規参入企業には、ハードルは高いでしょう。
- YB2/0細胞での生産性(?)
- 不純物等に関わる安全性の実績(?)
- レギュレトリーでのハードル(?)
- 市販に対応できる自社及委託先の製造設備と技術
高い細胞傷害活性を有する抗体医薬品の YB2/0 細胞を用いた効率的な物質生産研究 2011
https://gair.media.gunma-u.ac.jp/dspace/bitstream/10087/6623/1/Ph.D%20E-428.pdf
セルラインの種類
研究用としては、以下のように種々の細胞株が使われます。Creative Labより
- CHO cell lines: GS system, DHFR system;
- BHK cell line;
- Mouse myeloma cell lines: NS0, SP2/0, etc.
- Rat myeloma cell lines: YB2/0, etc.
- Human cell lines: HEK293 and its derivatives, HT-1080, Huh-7, PER.C6 , etc.
以上
編集履歴
2020/05/23 はりきり(Mr) 2020/06/09 文言整備 2020/06/20 追記 (細胞株、日本で市販される抗体医薬の細胞株の数) 2020/08/05 追記 (ヒト化抗体)
2022/10/23 文言整備: Fc領域の活用による機能付加について -
![[Bio-Edu] Fcエフェクター活性 – ADCC活性を増強するafucosylation技術 [2020/05/22]](data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAB4AAAAU9AQAAAAA2EmbpAAAAAnRSTlMAAHaTzTgAAAFQSURBVHja7cEBDQAAAMKg909tDjegAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAA4M7qkAAXe1B3gAAAAASUVORK5CYII=)
[Bio-Edu] Fcエフェクター活性 – ADCC活性を増強するafucosylation技術 [2020/05/22]
ID15631
はじめに
ADCC活性は、NK細胞などの免疫エフェクター細胞(immune effector cells)上に存在する抗体のFc領域に対するレセプターであるRcγRIIIaが関与しています。
IgG1のFc領域は、FcγRIIIaと結合親和性があり、その結合強度によってADCC活性が増強されます。この結合親和性の強さに影響するのが、Fc領域の糖鎖です。一般的にFc領域には、糖鎖結合部位がありますが、付加されている糖鎖として「フコース; fucose」含有量が少なければ、立体構造上から結合力が増加してADCC活性(エフェクター機能)が高まることが知られています。
fucoseは、Fc領域の糖鎖負荷領域のN型結合グリコシル(N-linked glycosylation)に付加されます。
ADCC活性とCDC活性
抗体のFc領域を介した生体反応は、(1) IgG1のFc領域と補体系のC1分子と作用する古典経路の活性化を惹起します(CDC)。また、(2) IgG1のFc領域とFc受容体(FcγIIIa)を介して貪食細胞の動員による作作用経路の活性化(ADCC)を惹起します。
- CDC (complement-dependent cytotoxicity)
- ADCC (Antibody-dependent cell-mediated cytotoxicity)
FcとRcγレセプターの結合親和性
FcγIIIaは、Fc領域にあるヒンジ部とCH2ドメインと相互作用します。
この相互作用は、CH2ドメインのAsn297 (N297)に付加される糖鎖構造に左右されます。この糖付加をできなくするアミノ酸の変異により、FcγRIを除くFcγRs (FcγRII, FcγRIII)への結合親和性は完全に消失します。
ヒトにおける天然のIgGの付加糖鎖は非常に不均一です。そのfucosylation研究では、フコシル化(afucosylation)のレンジは、1.3%~19.3%でした2)。CHO細胞から作られているモノクローナル抗体のフコシル化は、90%程度です。この差によるADCCやCDCに関わる活性の違いが生じています。
FcγIIIの遺伝子は2つ
FcγIIIの遺伝子は、2つあり、FcγIIIa (細胞の膜貫通型;殆どのエフェクター*)細胞で発現 )とFcγIIIb (好中球でのみGPIアンカー型タンパク質として発現)です。その配列相同性は97%ですが、FcγIIIbのADCCはありませ。しかし、貪食に関する役割を持つ可能性があります。
- FcγIIIa (殆どのエフェクター細胞)
- FcγIIIb (好中球のみ)
編集履歴
2020/05/22 はりきり(Mr) 参考文献1)を基に解説FcγIIIaの対立遺伝子*)には、Val(V158)とPhe (F158)が知られていますが、FcγIIIa-V158では、より高いIgG1結合親和性(10倍)を持っています。anti-epidermal growth factor receptor (EGFR)、anti-CD20で、その観察結果が出ています。
- V185
- F185
関連する抗体医薬 (ADCCによる癌細胞の破壊)
Protein fucosylation in mammalian system
Fucose (6-deoxycholate-L-galactose)は、哺乳動物細胞におけるN及びO型グリカンの共通成分です。
Fucose付加反応を担う酵素は、ヒトでは13種類のフコシルトランスフェラーゼ : FUT (fucosyltransferase)が知られています。
FUTは、fucose residue (フコース残基)をGDPフコース (GDP-β-L-フコース: 細胞室内(cytoplasm)で合成、フコシル化反応の基質)からアクセプター基 (acceptor substrate)に転移します。
細胞室内のGDP-fucoseの合成には、de novo経路が大半を担い、salvage pathway (生体でのフコースの再利用)はその一部を担っています。
- de novo回路 → GDP-fucose → (cytoplasm) → fucose residue
de novoは更に、GDP-mannoseからGDP-fucoseに変換する反応も担っています。
- GDP-mannose →(by GDP-mannose 4,6 dehydrates (GMD) and GDP-keto-6-deoxymannose 3,5-epimerase/4 reductive)→ GDP-fucose
- GDP-fucose → ( Golgi apparatus or endoplasmic reticulum (ER) )
- GDP-fucose transporter (GFT), encoded by the Slc35cl gene (Solute Carrier family 35), この遺伝子の変異は、白血球接着不全II型(LADII)、重度の免疫不全、精神遅滞、成長鈍化(グリコシル化IIc型の先天疾患)の発症につながります。
FUT 機能 1 fucose residue →(転移)→ terminal galactose
α1,2 linkageの形成2 同上( same as above) 3 α1,3/α1,4 – fucosyltrasferase (Lewisa, Lewisb合成と関連構造に関わる)反応 4 – 7 α1,3 – fucosyltransferase (ABHとLewis抗原の合成) 8 α1, 6 – fucosyltransferase (fucose – innermost(最も内側) N-acetylglucosamin on N-glycans)
肝臓以外の組織で広く発現しているが、肝細胞癌 (HCC)でアップレギュレーとされる9 – 11 α1,3 – fucosyltransferase (ABHとLewis抗原の合成) (POFUT1) O-fucosyltransferase
Ser/Thr残基にfucoseを直接付加 (ER内)(POFUT2) O-fucosyltransferase
Ser/Thr残基にfucoseを直接付加 (ER内)ガン抗原としてのLewis構造
Lewis抗原は、癌細胞が血管内皮 (vascular endothelium)へ接着する際に機能します(血行性移転)
Lewis関連の3糖または4糖 (ルイス抗原)は、炎症反応におけるリンパ球のホーミング中に白血球の接着に重要な役割を果たします。
Lewis構造
- ルイス抗原 type-1 (Lewis)
- Lewisa (Lea)
- sialyl-Lewisa (SLea) : ガン抗原CA 19-9と共に腫瘍マーカーとして一般的に使用
- Lewisb (Leb)
- ルイス抗原 type-2 (Lewisb)
- Lewisx (Lex)
- sialyl-Lewisx (Slex)
- Lewisy (Ley) : ヒトの消化管粘膜のO型結合グリカンと類似
ADCCの増強
- 抗体のFc領域 – FcγRIIIa の結合をトリガーとする
- FcγIIIaを持つ免疫細胞は、NK細胞
- 標的細胞を殺すサイトカイン/細胞溶解剤の放出
- ADCC活性は、FcのN-グリカンの影響を受ける
- CHO細胞由来のIgGでは、そのN-グリカンのコア位置に付加されたフコース残基は、異種の2分岐複合型であり、N-グリカンには、シアル酸は殆ど含まれない
- G0 galactose residue
- G1 galactose residue
- G2 galactose residue
- CHO Lec13細胞由来IgG1抗体と野生型CHO細胞由来との比較研究では(Shields er al.)、
- CHO Lec13細胞は、GMD遺伝子変異があり、非フコシル化N型糖鎖の含有率が高い
- CHO Lec13細胞で作ったIgG1のFcγIIIaへの結合親和性は、50倍増強(NK細胞/PBMC)
- ガラクトースやバイセクティングGlcNacの存在ではなく、フコースの不存在がADCCを高める(Shinkawa er al.)
- 別の研究では、コアフコースの除去が最大のADCC活性をは達成すると示唆した (コアフコースの除去と、S229D / D298A / I1332Eのミューテーションでは、ADCC活性の増強の差は無かった)
- FcγRIIIのアミノ酸変異 (Asn162Gly)とIgGとの結合研究によるADCC活性の増強の比較
- IgG-フコースフリーとFcγRIIIa-Asn162 >> IgGネイティブグリカンとFcγRIIIa-Gln162 > IgGネイティブグリカンとFcγRIIIa-Asn162
- IgG-フコースフリーとFcγRIIIa-Asn162 >> IgGネイティブグリカンとFcγRIIIa-Gln162 > IgGネイティブグリカンとFcγRIIIa-Asn162
- Fcのガラクトシル化とシアリル化によるADCC増強は、コアフコース除去と比較して限定的だが、Alanineスキャンにより増強効果が確認された。
- Fcエンジニアリング(IgG1)
- FcγRIIIaとの相互作用最大1倍の増強(増強しない)(T256A、K290A、S298A、E333A、K334A)
- FcγRIIIaとの相互作用最大169倍 (S239D or I332E、S239D and I332E、S239D and I332E and A330L
- 「活性化FcγRIIIa」と「阻害性RcγRIIb」との結合比を最大9倍 (S239D and I332E and A330L): Xencorによるヒト化の抗CD19抗体(XmAb5574: 広範囲のBリンパ腫および白血病の細胞株に対するADCC活性増強、患者由来急性リンパ牙球性白血病とマントル細胞リンパ腫細胞のタイルADCC活性増強)
afucosilated 抗体の生産戦略
GDP-fucoseの生合成酵素
CHO Lec13細胞は、内因性(endogenous)のGDP-mannose 4, 6 – dehydratase (GMD) 遺伝子を欠乏しています。GMDは、de novo GDP-2 fucose生合成3経路 (biosynthesis pathway)の最初のステップの触媒を担っています。
GMD遺伝子を欠乏しているにも関わらず、フラスコ培養で培養した結果、フコシル化抗体の比率は、50~70%になったという研究があります。
mRNAレベルでGMDが少なからず発現しており、別の発現パスウェイがあると考えられます。
GDP-keto-6-deoxymannose 3,5-epimerase/4 reductive (FX) – ノックアウト CHO細胞を用いて、完全にフコシル化を抑えたという研究もあります。
FUT8
Fut8遺伝子の発現レベルが低いYB2/0細胞を使用した研究 (CHO細胞との比較, Arakawa er al.)
- humamized anti-human interleukin-5 receptor (IL-5) IgG1 antibody (KM8399) in YB2/0 cell
- core fucose of KM8399 was lower level
- 産生したIgG1は、いずれの細胞でも同様の抗原結合性を示した
- YB2/0細胞由来では、コアフコースのレベルが低くく、ADCC活性は、約50倍であった
- YB2/0細胞のFUT8 mRNAレベルは、有意に低くかった
FUT8遺伝子の不活化(Yamane er al.)
- 抗CD20抗体産生CHO細胞 DG44細胞株
- FUT8対立遺伝子ともにゲノム領域からのノックアウト(FUT8 -/-)
- 同様の培養増殖曲線と、同様の生産性
- 完全な非フコシル化抗体の産生
- 親株との比較で2倍のADCC増強
siRNAを使用したCHO DG44細胞の培養
- 60%の非フコシル化抗体の産生
CHO細胞のGDP-fucose transporter (GFT)を除去
- ゴルジ体のGDP-fucose transporter (GFT)遺伝子(Slc35c1)のノックアウトによるゴルジ体でのフコシル化反応を止める
- zinc-finger mucleases (ZFNs)、transcription activator-like effector nucleases (TALENs)及びCRISPR-Cas9、などの技術を用いた
- fluorescence-activated cell sorting (FACS)で分別 (Aleutian aurantia lectin (AAL) )
- 得られた細胞は、CHO-gmt3 (CHO-glycosylation mutant3)
- EPO-Fc融合タンパク質とIgG1抗体において、core fucoseは、完全に欠落していた
- この手法により、無血清培地、細胞増殖率、生存細胞密度についての安定株を2ヶ月で樹立することが可能
- CHO-K1細胞は、そのtranscriptome dataから、Golgi fucosyltransferaseの内、FUT8のみを発現していることが示されています
- Fut8よりもSut35c1をノックアウトする方(Stc35c1 -/-)が利点があると筆者は述べています。
- CHO細胞に適用した結果、培養増殖率、生存率、抗体産生などが同等であった
Bisecting GlcNac
β-1, 4-mannosyl-glycoprotein 4-β-N-acetylglucosaminyltransferase (GnT-III)は、普通CHO細胞では発現されません。
以下の2つの過剰発現のCHO細胞株は、抗CD20抗体GA101の宿主株として成功しています。最高レベルの(1) bisecting、(2) afucosylated glycansを、IgGで実現しました
- GnT-IIIの過剰発現
- これのみでCHO細胞でのFcコアのフコシル化が減少
- Golgi α-mannosidase II (αManII)の過剰発現
GnT-IIIは、以下を触媒します。
- 以下を結合 (β1,4)させて、bisecting GlcNAcを作る
- GlcNAc
- N-glycansのtrimannosyl coreのβ結合型mannose
GDP-フコース de novo経路
[GDP-fucose de novo(advice)経路]では、GDP-mannoseは、GKDMに変換される。
- GDP-mannose → (GDP-mannose-4,6-dehydratase)→ GDP-4-keto-6-deoxy mannose (GKDM)
- GKDM → (several downstream emzymatic reactions) →GDP-fucose
[バクテリア]では、GKDMはGDP-rhamnose形態に還元できます。GDP-rhamnoseは、細菌の一般的な細胞膜表面グリカンの1種です。
- GKDM → (GDP-4-keto-6-deoxy mannose reductase (RMD) )→ GDP-rhamnose
[CHO細胞]の細胞質内に、このRMDを異種発現することで、[GDP-Fucose de novo経路]がバイパスされるため、afucosylated IgGが作られます。最終産物であるGDP-rhamnoseは、GMDの阻害剤である可能性があります。
- GKDM → (GDP-4-keto-6-deoxy mannose reductase (RMD) )→ GDP-rhamnose
フコシル化阻害剤
遺伝子改変ではないアプローチとして、Okeley et al.による阻害剤研究があります。
- 2-fluorofucose
- 5-alkynylfucose
その作用機序は、以下のことが考えられます
- 細胞内GDP-fucoseの枯渇化 → de novo経路の遮断
- FUT8の阻害
植物細胞と後処理
植物細胞の利用
植物細胞では、以下の糖鎖が欠落します。
- α1,6-fucose
- β1,4-galactose
- α2,3-sialic acid
植物細胞では、通常、N-glycanは、(1)以下の糖鎖が付加されますが、(2)大きな糖鎖(哺乳動物でも稀に見られる)が付加されることもあります。
- Man3GlcNAc2コアに以下のもので糖鎖修飾
- β1,2-xylose ( mammalian では不要であり免疫原性がある)
- コアxhloseは、献血ドナーから抗体が検出される
- α1,3-fucose
- この糖鎖を含むGnGnXF3構造(免疫原性)
- コアα1,3-fucoseは、健常人献血ドナーから抗体が検出される
- β1,2-xylose ( mammalian では不要であり免疫原性がある)
- Large complex type N-glycans
- Lewisa構造
- α1,4-fucose
- β1,3-galactose
- Lewisa構造
Strategy to overcome this immunogenicity
植物由来の糖鎖の免疫原性を克服するには、以下戦略があります。
- RNAi knockdown of α1,3-fucosyltransferase (FucT) in plant
- β1,2-xylosyltransferase (XylT) in plant
- FucT/XylT-knowckout lines
水草のLemna minorで作ったafucosylated anti-CD30 monolclonal antibody
- 得られたG0構造のこの抗体は、CHO細胞由来と比べてADCC活性が改善されました
Anti-HIV 2G12 from XylT/FucT – knockdown N.benthamiana
- 得られたG0構造は、N-acetylglucosamine末端において、以下の糖鎖を欠落してさせることができました
- xylose
- α1,3-fucose
付加糖鎖を後処理で除去
- endo-β-N-acetylglucosamidaseなどのEndo SでN-glycanを切断
- その後、exoglycosidaseであるfucosidaseで、core fucoseを除去
- 残ったmono-GlcNAcは、不均一であるので、desialylated complex型のoxazolineの存在下、Endo Sベースのglycosynthases(グリコシンセターゼ)によるtransglycosylation (糖転移反応)を行う
- この方法は、コストがかかります
治療用のafucosylated mAbs
2018年現在で、3つのafucosylated mAbsが市場に、20以上が臨床試験にあります。
name and company Target andformat comment obinutuzumab/GA101/Gazyva
RocheCD20
Humanized IgG1 with low fucose contentMarketed
first glycoengineered therapeutic anti-CD20, in 2013 by FDA
3 x Phase 1~3mogamulizumab/POTELIGEO/KM0761
Kyowa Hakko KirinCD chemokine receptor 4(CCR4) Humanized afucosylated IgG1 Marketed in lymphoma
first approved in 2013 in Japan for hematologic malignancies
in 2014 for cutneous T-cell lymphoma (CTCL)
in 2017, FDA granted itbreakthrough, FUT8-knockout CHO
10 x Phase1~3Benralizumab/MDEI-563/Fasenra
AstraZenecaIL-5Rα
Humanized afucosylated IgG1Marketed in Asthma
approved by FDA in 2017 for severe eosinophil asthma, FUT8-knockout CHO (Biowa Poteligent Technology), IL-5R
9 x Phase1~3Inebilizumab/MEDI-551
MedlmmuneCD19
Humanized afucosylated IgG110 x Phase1,2 and 3 (lymphoma,myeloma) Ublituximab/TG1101/LFB-R603
TG Therapeutics IncCD20
Chimeric IgG1, low fucose content10 x Phase 1,2 and 3 in lymphoma, leukemia TrasGEX/GT-MAB7.3-GEX/Glycooptimized Trastuzumab-GEX HER2
Mumanized glyco-optimized (reduced fucosylated IgG1)Solid Tumors in Phase 1 (completed) SEA-CD40/Seattle Genetics humanized afucosylated anti-CD40 IgG1 Cancer and carcinomas in Phase 1 その他多数、原書を参照のこと 以上
参考文献
1)
The “less-is-more” in therapeutic antibodies: Afucosylated anti-cancer antibodies with enhanced antibody-dependent cellular cytotoxicity, 2018
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6150623/2)
Glycosilation engineering of therapeutic IgG antibodies: challenges for the safety, functionality and efficacy
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5777974/#!po=7.608703)
Improved in vitro and in vivo activity against CD303-expressing targets of the chimeric 122A2 antibody selected for specific glycosylation pattern, 2018
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5973763/4)
細胞性免疫・エフェクター細胞 – 日本ガン免疫学会
http://jaci.jp/patient/immune-cell/immune-cell-04/5)
対立遺伝子
https://mycode.jp/glossary/allele.html編集履歴
2020/02/22, by Mr.Harikiri
-
![[Edu] Creative Biolabs Inc.が公開しているビデオから – COVID-19の原因ウイルスである新型コロナウイルス(SARS-CoV-2)の構造について学ぶ [2020/05/21]](data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAB4AAAAU9AQAAAAA2EmbpAAAAAnRSTlMAAHaTzTgAAAFQSURBVHja7cEBDQAAAMKg909tDjegAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAA4M7qkAAXe1B3gAAAAASUVORK5CYII=)
[Edu] Creative Biolabs Inc.が公開しているビデオから – COVID-19の原因ウイルスである新型コロナウイルス(SARS-CoV-2)の構造について学ぶ [2020/05/21]
CROの宣伝ビデオ
Creative Biolabs Inc.というCROが、アメリカのニューヨークに本社を構えています。このCROについて調査している過程で、宣伝ビデオを沢山公開していることを知りました。非常に参考になるのでご紹介します。
COVID-19は、SARS-CoV-2という新型コロナウイルスが引き起こす病気の名前です。
今回は、SARS-CoV-2というウイルスの構造について、Creative Biolabs Inc.がYouTubeに公開しているビデオから解説します。
編集履歴
2020/05/21 はりきり(Mr)新型コロナウイルスの構造
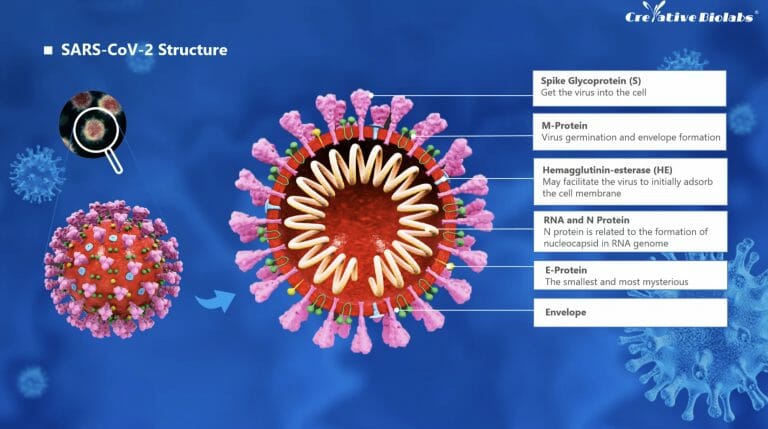
新型コロナウイルスの正式名称は、SARS-CoV-2と言います。1本鎖プラス鎖RNAウイルス、RNA長は29.9kbです1)
- Spike Glycoprotein (S) 3)
- M-Protein 4)
- エンベロープ(Envelope)を構成するタンパク質
- メンブラン(M)タンパク質
- 発芽(Release)、形態形成とアセンブリに関連する
- Hemagglutinin-esterase (HE) 6)
- 赤血球凝集エステラーゼ
- 初期の吸着メカニズムを構成する当タンパク質
- 細胞表面のシアル酸受容体への吸着とその破壊に関わる
- N Protein 4)
- ヌクレオカプシド(N)タンパク質
- ウイルスのエンベロープ内のウイルスRNAゲノムを、カプシドと呼ばれるリボ核タンパク 質(RNP)複合体にパッケージ化することに関わる
- E-Protein 4)
- エンベロープ(Envelope)を構成するタンパク質
- 小さいタンパク質であり、よくわかっていないが、アセンブリ、出芽、エンベロープ形成、病原性に関連するとされる
- Envelope 2)
- M-ProteinやE-Protein以外の膜成分であり、宿主由来の脂質や膜タンパク質

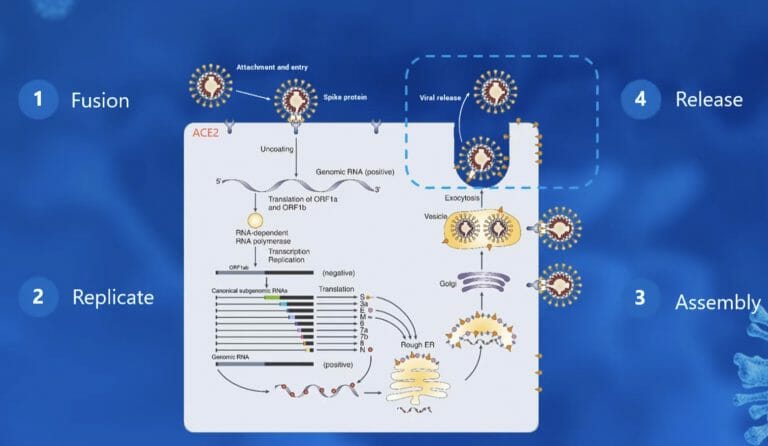
感染と増殖
- Fusion
- HEと宿主プロテアーゼ
- RNA genomeが注入される
- Replicate
- 細胞質内
- Assembly
- 小胞体、ゴルジ体で成熟
- Release
- 出芽

参考ビデオ (Create Biolabs Inc.)
是非、英語の解説をビデオでご覧になってください。
以上
参考文献
1)
新型コロナウイルスSARS-CoV-2のゲノム分子疫学調査 (2020/4/16現在)
https://www.niid.go.jp/niid/images/research_info/genome-2020_SARS-CoV-MolecularEpidemiology.pdf2)
エンベロープ(ウイルス)
https://ja.wikipedia.org/wiki/エンベロープ_(ウイルス)3)
コロナウイルスの構造 – 岩井科学薬品株式会社 – より
https://www.iwai-chem.co.jp/products/sinobiological/sars-cov-2/4)
ウイルス学研究用 新型コロナウイルスSARS-CoV-2 構造タンパク質 – BioVendor – より
https://filgen.jp/Product/Bioscience4/BioVendor/BioVendor_SARS-CoV-2-protein_flyer.pdf5)
プロテアーゼ依存的なコロナウイルス細胞侵入 – ウイルス 第61巻 第1号 – より
https://filgen.jp/Product/Bioscience4/BioVendor/BioVendor_SARS-CoV-2-protein_flyer.pdf6)
Hemagglutinin esterase – Wikipedia – より
https://en.m.wikipedia.org/wiki/Hemagglutinin_esterase -
![[Bio-Edu] バイオ医薬品におけるウイルス・クリアランス試験 – モニターウイルス – 除去率 – [2020/08/23]](data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAB4AAAAXQAQAAAACcyG61AAAAAnRSTlMAAHaTzTgAAAFxSURBVHja7cEBAQAAAIIg/69uSEABAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAPBoeRsAAWhLowEAAAAASUVORK5CYII=)
[Bio-Edu] バイオ医薬品におけるウイルス・クリアランス試験 – モニターウイルス – 除去率 – [2020/08/23]
はじめに
Biologics (生物製剤)では、混入する可能性のあるウイルスについてリダクション能力を評価していることが必要であり、商用製品では、製造工程のウイルス・クリアランス試験が必須である*1。臨床サンプルについてもウイルス・クリアランス試験として、1~2種類のモデル・ウイルスを用いて実施されているのが実情である。
ウイルス・クリアランス試験には、(1) エンベロープを有し比較的耐久性の低いレトロウイルスのモデル・ウイルスとしてX-MLV (MuLV: Xenotropic murine leukemia virus)、(2) エンベロープを持たず小型で耐久性の高いパルボウイルスのモデル・ウイルスとしてMVM (minute virus of mice:MVM = murine minute virus:MMV = Murine parvorirus source)の使用が多い。
- MLV (MuLV; MMLV) source:wiki
- MVM; Murine Minute Virus, MMV; Mice Minute Virus, Murine Parvovirus
編集履歴 2020/05/18 はりきり(Mr) 2020/05/25 追記(ウイルス除去工程) 2020/08/23 充実化(ウイルス除去工程)
製造工程のウィルス・クリアランス試験など、求められる試験 – Eli Lilly and Company, CMC Strategy Forum, Europe, 2018 – より
Modular Retrovirus Clearance in Support of Clinical Development, Bio-product Research & Developmentウイルス記号 ゲノム エンベロープ サイズ (nm) 抵抗性 ネズミ白血病ウイルス MuLV *2 single stranded RNA (+) 80 – 110 低い マウス微小ウイルス MVM single stranded DNA (-) 18 – 24 非常に高い ウイルスクリアランス事件の課題と事例検討 — 総ウィルスクリアランス指数(LRV)をどこまで追求するか — PDA Journal of GMP and Validation in Japan Vol.7, No.1 (2005) MLVのRNAをqPCRで定量
ウイルス・クリアランス試験
一般的なウイルス除去工程
- 培養終了後のハーベスト
- 清澄ろ過膜にAEXモードを持つフィルター機材を採用している場合は、ウイルス除去効果が期待される
- Affinity Chromatography
- 抗体医薬では、Protein Aのアフィニティ・カラムクロマト工程によるウイルス除去効果が期待される
- AEX Chromatography
- 陰イオン交換カラムクロマトの不純物除去工程によるウイルス除去効果が期待される
- CEX Chromatography
- 陽イオン交換カラムクロマトの不純物除去工程によるウイルス除去効果が期待される
- Virus reduction Filtration
- ウイルスの除去を目的としたウイルス除去ろ過工程
- Planova 20NやViresolveが使用される
評価方法
- 除去率(Reduction Level; RL)は、Log10で表記
- 各工程で、ウイルスの添加回収実験の実施
- 各工程でのRLの総和を求めて、製造工程全体のクリアランス能力を算定する
- 細胞アッセイ
- 動物への投与
- PCR
- など
ウイルス除去率の解釈
関連するガイドラインには、ウイルスの除去率に関して考慮すべき要因が示されています1)。以下の要因について考慮することで、プロセスステップをウイルスの不活性化/除去において、以下のように見なすことができるかどうかを決定します
- 有効
- 適度に有効
- 無効
考慮する要因
- 使用したテストウイルスの適切性(セクション4を参照/工事中)
- 検証研究の設計(セクション5を参照/工事中)
- 除去率
- 4 logまたはそれ以上の削減は、モニターウイルスにおいて明確な効果を示していると言える
- 4 logまたはそれ以上の削減は、モニターウイルスにおいて明確な効果を示していると言える
- 不活化の速度論
- 不活化は通常、単純な一次反応ではなく、多くの場合、最初の段階が速く、その後に遅い段階があります。 ただし、時間とともに不活性化率が劇的に低下する場合は、不活性化剤の有効性が失われていること、または残存ウイルス画分が不活性化剤に耐性があることを示唆している可能性がある
- 不活化は通常、単純な一次反応ではなく、多くの場合、最初の段階が速く、その後に遅い段階があります。 ただし、時間とともに不活性化率が劇的に低下する場合は、不活性化剤の有効性が失われていること、または残存ウイルス画分が不活性化剤に耐性があることを示唆している可能性がある
- 不活化/除去の性質
- および特定のクラスのウイルスに対してのみ選択的かどうか。 プロセスステップは、一部のウイルスに対しては非常に効果的ですが、他に対しては効果がありません。たとえば、S / D処理は、脂質を含むが脂質を含まないウイルスに対しては効果的です
- および特定のクラスのウイルスに対してのみ選択的かどうか。 プロセスステップは、一部のウイルスに対しては非常に効果的ですが、他に対しては効果がありません。たとえば、S / D処理は、脂質を含むが脂質を含まないウイルスに対しては効果的です
- プロセスパラメータの小さな変動に対するウイルスの不活性化/除去の影響は、ステップの信頼度に影響する
- アッセイ感度の限界
何回か試験を実施して、異なる除去率が計算された場合、リスクを考慮して評価するなら低い方の値を採用する。
ウイルス・アッセイの例示
ウイルス・アッセイについて、以下の文献から例示として情報を抽出した。ウイルスに応じて感染効率の高い細胞を使用し、用いる細胞の培養に使用する培地についても参考になる。
Cell
- S+L- cell line on semisolid agar colony
- 3T3FL cell for SV assay
- C-182 cell line, a mixture of apparently normal 3T3FL cells and S+L- cells for MuLV assay
media
- McCoy’s 5a medium ( Grand Island Biological Co., Grand Island, N.Y.), 10% FCS and antibiotics
- Eagle’s minimum essential amino acids
- 10% FCS, antibiotics, 20mM thymidine
- (Phenol Redを入れない場合が多い)
Virus (MLV)
- Moloney leukemia virus (MLV) from Electro-Nucleonics Laboratories, Inc., Bethesda, Md., as crude tissue culture fluid from MSV infected JLSV9 cells
- 5 x10E5 FFU/mL to use for the superinfection of S+L- cells.
- MLV from University Laboratories, Highland Park, N.J., as 10% spleen suspension from MLV-infected mice.
- to use for the MSV assays as leukemia helper virus
Virus assays
- A rapid cell culture assay technique for MuLV
- induction of foci in S+L- cells with superinfection
- MSV focus-forming assay
- Both sample are prepared
- by freezing and thawing 3 times cells and supernatant fluids together followed by low-speed centrifugation to remove cell debris.
- stored at -70 C prior to virus assays
追記
ウイルス液の清澄化は、低いGでの遠心上清、超遠心で濃縮する。
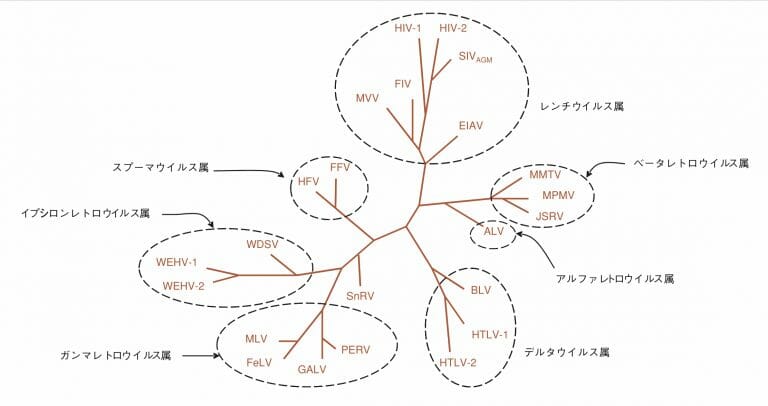
レトロウイルス・系統樹
図1(左)の系統樹をもとに、以下詳細にまとめた。
- レンチウイルス属
- EIAV (equine infectious anemia virus), ウマ
- MVV (Mahdi-Visna virus), ヒツジ、ウマ
- FIV (feline immunodeficiency virus), ネコ(免疫不全)
- HIV-1
- SIVAGM
- HIV-2
- スプーマウイルス属
- FFV (feline foamy virus),ネコ,
- HFV
- アルファレトロウイルス属
- ALV (avian leukosis virus),トリ
- ベータレトロウイルス属
- MMTV (Mouse mammary tumor virus), マウス
- JSRV (jaagsiekte sheep retrovirus), ヒツジ,
- MPMV
- ガンマレトロウイルス属
- MLV (murine leukemia virus; マウス白血病ウイルス), マウス
- E-MLV (ecotropic:同種指向性)
- X-MLV (xenotropic:異種指向性)
- FeLV (feline leukemia virus), ネコ
- GALV
- PERV (porcine endogenous retrovirus), ブタ
- MLV (murine leukemia virus; マウス白血病ウイルス), マウス
- デルタウイルス属
- BLV (bovine leukemia virus)、ウシ
- HTLV-1
- HTLV-2
- イプシロンウイルス属
- WDSV
- WEHV-1
- WEHV-2
- SnRV

5. 動物由来レトロウイルスの受容体、ウイルス 第 59 巻 第 2 号,pp.223-242,2009 
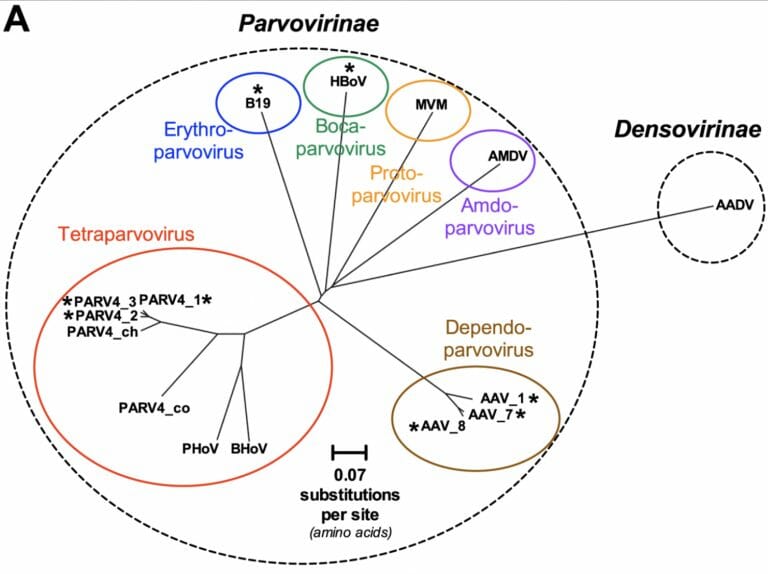
パルボウイルス・系統樹
- Proto-parvovirus
- MVM (minute virus of mice)
- Boca-parvovirus
- HBoV
- Erhthro-parvovirus
- B19
- Amdo-parvovirus
- AMDV
- Tetraparvorirus
- BHoV
- PHoV
- PARV4_co
- PARV4_ch
- PARV4_2
- PARV4_3
- PARV4_1
- Dependo-parvorirus
- AAV_1
- AAV_7
- AAV_8

感染様式
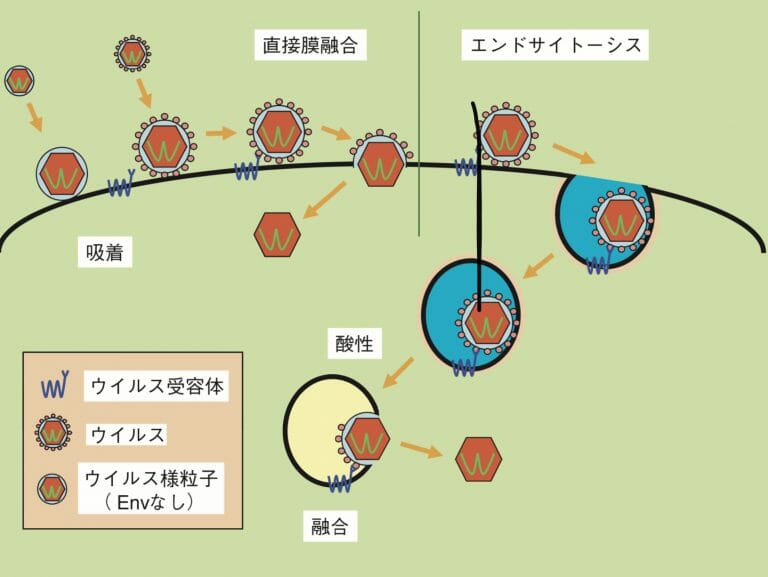
レトロウイルスの感染様式
図1(右)は、レトロウイルスの感染様式を示している。
先ず、レトロウイルスは、細胞表面に非特異的に吸着し、その後、以下の機構のいずれかで細胞内に進入する
- 非特異的吸着
- レトロウイルスのエンベロープと細胞表面の受容体が結合
次に細胞質内に以下の機構により侵入する
- 直接膜融合
- エンベロープの構造変化により、エンベロープを除くウイルス様粒子が、細胞質内取り込まれる
- エンドサイトーシス
- エンベロープごと裏返った細胞膜に覆われて、細胞質内に取り込まれる(エンドソソーム)
- 直接膜融合により、エクンドソームから飛び出し、細胞室内に移動する。
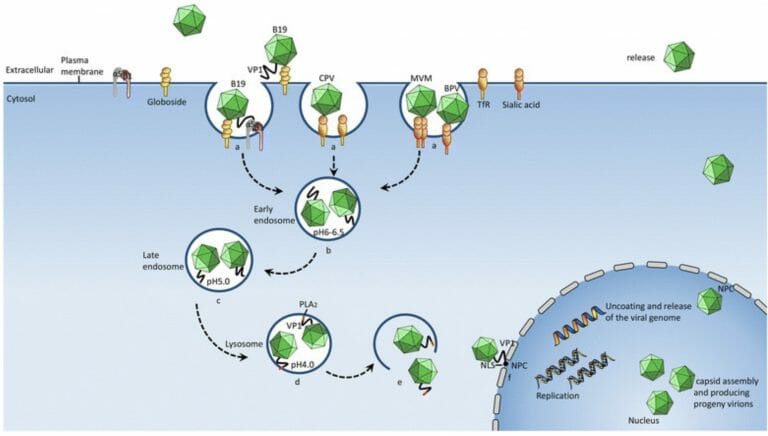
パルボウイルスの感染様式
パルボウイルスは、細胞表面に吸着した後、endocytosisで細胞質内に入ります。その後、endosomeは、内部がpH4になったLysosomeに変換され、同時にphospholipase A2を活性かされて、Lysosomeの膜を破り、ウイルス粒子は細胞質内にでできます。その後、VP1を介して細胞核に入り込まれてゆきます。

1) ガイドライン
以上
- MLV (MuLV; MMLV) source:wiki
-
![今日の英語 – 丁寧にお礼する – I would like to thank you for … [2020/05/18]](data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAB4AAAAU9AQAAAAA2EmbpAAAAAnRSTlMAAHaTzTgAAAFQSURBVHja7cEBDQAAAMKg909tDjegAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAA4M7qkAAXe1B3gAAAAASUVORK5CYII=)
今日の英語 – 丁寧にお礼する – I would like to thank you for … [2020/05/18]
I would like to thank you for …
…について感謝したいと思います。編集履歴 2020/05/18 Mr.HARIKIRI
-
![[Trip] イギリスのウインザー城門前 – フィッシュアンドチップスが美味い THE CARPENTERS ARMS (2016) [2020/05/17]](data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAArAAAAMAAQAAAAD0gmnaAAAAAnRSTlMAAHaTzTgAAABXSURBVHja7cEBAQAAAIIg/69uSEABAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAwK8BBQ8AAZG/36UAAAAASUVORK5CYII=)
[Trip] イギリスのウインザー城門前 – フィッシュアンドチップスが美味い THE CARPENTERS ARMS (2016) [2020/05/17]
THE CARPENTERS ARMS
イギリスのウインザー(Windsor)城の門前町にある、THE CARPENTERS ARMS (ザ・カーペンターズアーム)は、ビールはもちろんですが、ボリュームあるフィッシュアンドチップスが美味い。
ウインザーは観光地だけあってゆったりと時間が流れます。数日の滞在でも毎日でも行きたい、UKを満喫できるディナーのとっておきの店です。
編集履歴 2016 Trip 2020/05/17はりきり(Mr) 2021/09/03,追記(通過)
ウィンザー城




店構え
日も暮れてお腹も空いた頃です。気候が良ければ、お客は店前のテーブルでビールを飲み、楽しそうに語らっています。この辺りは、食事する店は沢山あり困ることはありません。今日は、THE CARPENTERS ARMSにしましょう。




フィッシュアンドチップス
単価は日本と比べて同程度か少し高いかも知れませんが、ボリュームがあるので、カップルで食事する場合は、1人前をシェアすればいいくらいです。節約になります。
フィッシュアンドチップスとサーモンサラダ。サラダの野菜は日本では食べたことのない葉っぱでしたが、クセはなくてイギリスを味わいました。



お勘定は、クレジットカードで良いですが、チップを払う項目もあります。支払いの5%から10%程度を払ったと記憶しています。
- UK: イギリス
- 通貨: ポンド(GBP; Great Britain Pound,£)/ペンス(Pence), 1£=100 pence
以上
-
![[Hotel] リーガロイヤルホテル大阪 – スイートルーム (2018) [2020/05/17]](data:image/png;base64,iVBORw0KGgoAAAANSUhEUgAAAwAAAAFOAQAAAAAZN0cWAAAAAnRSTlMAAHaTzTgAAAA2SURBVHja7cExAQAAAMKg9U9tDQ+gAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAAPgzfo4AAc/EnRoAAAAASUVORK5CYII=)
[Hotel] リーガロイヤルホテル大阪 – スイートルーム (2018) [2020/05/17]
リーガロイヤルホテル大阪
梅田にある「リーガロイヤルホテル大阪」のスイートルームに泊まったことがあります。
本館は、もう古いことと、平日を狙って宿泊日を決めたことで、格安で泊まることができました。
ロビー
2018年のロビーの絨毯は、今の新調した絨毯より小さい物でしたが、デザインは、現在の物へ踏襲されています。現在の絨毯は、ほぼロビーの一面を覆っています。
下の写真は、全体像を写すためにパノラマで撮影したため、手前の直線となるべき絨毯の一辺が曲線になっていますが、実際には直線で^^)
スイートルーム
広いリビングとベッドルーム

リーガロイヤルホテル大阪 





クラブラウンジ
夕食と朝食を頂きました。
窓からの風景


編集履歴 2018/08 宿泊 2020/05/17 Mr.HARIKIRI
![[用語] CDC ; Centers for Disease Control and Prevention; アメリカ疾病予防センター](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/09/0E1A8FDA-ABDA-4D42-811D-BE0041CBB6CB.jpeg)
![[WordPress] その昔憧れた、パーソナル・データベース生活を実現。 – イベント・プラグイン – を選定/導入する [2020/05/23]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/05/C964CF75-1E6C-4C3C-8638-46235FE5F388.jpeg)






![[Bio-Edu] バイオ医薬品 (バイオロジクス)は、CHO細胞の技術革新と共に進展してきた [2020/08/05]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/04/7913F478-4409-40B3-B393-A2F40B52CF99.png)
![[Bio-Edu] Fcエフェクター活性 – ADCC活性を増強するafucosylation技術 [2020/05/22]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/05/5754D002-C57A-4FC9-8992-BA71D66B5952.jpeg)
![[Edu] Creative Biolabs Inc.が公開しているビデオから – COVID-19の原因ウイルスである新型コロナウイルス(SARS-CoV-2)の構造について学ぶ [2020/05/21]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/03/6FA02902-6416-4379-954C-F2C73B68A651.jpg)
![[Trip] カリフォルニアのハロウィン・グッズ店のリアルな様子 [2020/05/20]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/05/F13BAFE1-B3C6-4C47-B441-FACB2A7EBEE2.jpeg)


























![[Bio-Edu] バイオ医薬品におけるウイルス・クリアランス試験 – モニターウイルス – 除去率 – [2020/08/23]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2019/07/41704B06-88E8-4AE5-BD78-83E866DDAED1.jpeg)
![今日の英語 – 丁寧にお礼する – I would like to thank you for … [2020/05/18]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/11/F12C8F86-A0B0-4334-9DAD-E75022893870.jpeg)
![[Trip] イギリスのウインザー城門前 – フィッシュアンドチップスが美味い THE CARPENTERS ARMS (2016) [2020/05/17]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/05/CB0E1EDA-62F5-4EAA-B118-2DD6CC9ACA2E.jpeg)










![[Hotel] リーガロイヤルホテル大阪 – スイートルーム (2018) [2020/05/17]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2020/05/0379D5ED-B208-4729-ACD3-BFF60C1C04D4.jpeg)









