今日は春分の日、お彼岸で、地下鉄サリン事件から30年でした。
両方の両親の墓参りをしてきました。昼飯をカレーして墓参りしてcafeで小腹に少し入れて、関西ストアで買い物して帰宅しました。

カレーはいつもの牛すじカレー。

鐘も吐いてきた。

オンカカビサンマエイソワカ・・・


一日中お疲れ様でした。
はりきり。
![お彼岸 – CoCo壱して墓参りの後にSunny-sideでcafeをして。今日一日お疲れ様。[2025/03/20]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2025/03/IMG_3602.jpeg)
今日は春分の日、お彼岸で、地下鉄サリン事件から30年でした。
両方の両親の墓参りをしてきました。昼飯をカレーして墓参りしてcafeで小腹に少し入れて、関西ストアで買い物して帰宅しました。

カレーはいつもの牛すじカレー。

鐘も吐いてきた。

オンカカビサンマエイソワカ・・・


一日中お疲れ様でした。
はりきり。
![[医薬品製造] 共用設備使用に関するガイドライン](https://harikiri.diskstation.me/myblog/wp-content/uploads/2021/02/80F3D755-3019-49C6-BDAE-47D137C87826.jpeg)
ガイドラインタイトル : Guideline on setting health based exposure limits for use in risk identification in the manufacture of different medicinal products in shared facilities (2014).
Copilot解説 :
「医薬品の製造におけるリスク識別のための健康に基づく曝露限界の設定に関するガイドライン」は、ヨーロッパ医薬品庁(EMA)が作成した文書で、異なる医薬品を共用設備で製造する際の交差汚染リスクを管理するための枠組みを提供しています。
![バイオ医薬品に不純物として含まれるDNAや核酸など,がん原性のリスクはないのか [2025/03/20]](https://harikiri.diskstation.me/myblog/wp-content/uploads/2021/02/80F3D755-3019-49C6-BDAE-47D137C87826.jpeg)
遺伝子治療で使用されるAAV製品などでは,断片化したDNAである不純物がある程度含まれる.この核酸の長さが一定以上あるとがん原性のリスクがあると一般的には言われている.以下,Copilotに聞いてみた.Copilotの以下の回答は妥当な回答になっている.
Q: DNAなど核酸が医薬品に含まれる場合,がん原性の懸念はあるか
Copilot : 医薬品にDNAやその他の核酸が含まれる場合、一般的にその量や形状、由来によって、がん原性の懸念が評価される必要があります。しかし、現在の科学的知見では、そのような懸念がある場合でも、厳格な基準や製造工程を通じて安全性が確保されています。
厚生労働省やPMDA(医薬品医療機器総合機構)を含む規制当局は、申請された医薬品の安全性データを審査し、がん原性のリスクが許容範囲内であることを確認しています。
総じて言えば、DNAや核酸の残存量が医薬品に含まれる場合でも、それらの管理が適切に行われることで、がん原性の懸念は最小化されています。
Q : 核酸やDNAの不純物の長さがある程度長いとがん原性のリスクが高まるのは本当か.理論的な話と実験的な結果からそういわれているのか
Copilot : 核酸やDNAの不純物が長い場合、がん原性のリスクが高まる可能性については、理論的にも実験的にも議論されています。ただし、具体的なリスクの評価は不純物の由来、量、長さ、そして体内での挙動など、さまざまな要素に依存します。
理論的には、DNAや核酸の長さがある程度長いとがん原性のリスクが高まる可能性が示唆されていますが、製造および品質管理の段階でこれらのリスクは非常に低減されています。実験的なデータも主に極端な条件下での結果が多いため、現実的なリスクは限られていると考えられます。
Q : がん原性が懸念されるDNAや核酸のヒトへの混入経路として皮膚や経口,静脈経由,皮下注射,筋肉注射など考えられるが,経路別のリスクについて教えて
Copilot : DNAや核酸の不純物がヒトに混入する経路別のがん原性リスクについて、以下のように整理します。各経路での体内吸収効率や生物学的バリアの有無に応じてリスクが変わります。
さらに具体的なケースや特定の医薬品に関連するリスクについて知りたい場合は教えてください!
がん原性が懸念されるDNAや核酸のヒトへの混入経路として皮膚や経口,静脈経由,皮下注射,筋肉注射,脊髄投与,など考えられるが,経路別のリスクについて教えて
DNAや核酸の不純物がヒトに混入する場合、経路別にリスクを評価すると以下のようになります。各経路は吸収効率、体内挙動、バリアの有無によってリスクが異なります。
以下に各経路のリスクをまとめます:
| 経路 | リスク | バリアの有無 |
|---|---|---|
| 静脈経路 | 高 | バリアなし |
| 皮下注射 | 中 | 局所的バリア |
| 筋肉注射 | 中~低 | 吸収速度が遅く影響は限定的 |
| 経口摂取 | 低 | 酵素と酸性環境による分解 |
| 皮膚経路 | 極めて低い | 健康な皮膚でほぼ完全なバリア |
| 吸入経路 | 低~中 | 粘膜と免疫系による防御 |
| 脊髄投与 | 高 | バリアなし(直接影響を及ぼす) |
各経路におけるリスク軽減には、製造工程での高度な精製と品質管理が不可欠です。
2025/03/20 Mrはりきり
![[医薬品] 医薬品の製造販売承認を受けた製販で必要となる文書と運営](https://harikiri.diskstation.me/myblog/wp-content/uploads/2021/02/80F3D755-3019-49C6-BDAE-47D137C87826.jpeg)
医薬品の製造販売承認を受けた製造販売業者(製販)は,組織や文書など体制を整えられている必要がある.基本的な組織や連絡体制,品質管理手順,製品ごとの品質標準書などを「医薬品、医薬部外品、化粧品及び再生医療等製品の品質管理の基準に関する省令」(Good Quality Practice;GQP省令)を中心に参照して整備されていなければならまい.以下のレジメは,Copilotを活用して細部をイメージしなが取りまとめた.経験上からは大きな齟齬がある内容ではないと思うが,実際にそうなっているのかについては未経験の部分もあるため細部が異なっている可能性が残る.全体的にはタイトルに挙げた目的に対しては,使用する用語や文書名,活動内容など,網羅できていると考えている.(Collaboration with Copilot!)
薬事法(昭和三十五年法律第百四十五号)第十二条の二第一号の規定に基づき、医薬品、医薬部外品、化粧品及び医療機器の品質管理の基準に関する省令を次のように定める。
医薬品、医薬部外品、化粧品及び再生医療等製品の品質管理の基準に関する省令
(平二六厚労令八七・改称)
GQP省令における「組織体制」に関する事項は、品質標準書や品質管理手順書には記載せず、別途「組織体制図」や「組織規程」として作成・管理することが適切です。「組織体制」に関する内容は、組織全体に関わる構造や責任分担を示すものであり、製品固有の情報を記載する品質標準書や運用手順を記載する品質管理手順書の範囲を超えるためです。
「組織体制」に関しては、以下のような文書を別途作成し、管理するのが一般的です:
GQP省令における「三役」とは、品質管理および品質保証体制の中核を担う三つの主要な役職を指します。それぞれの役割と責務は以下の通りです:
これらの役職は、それぞれが明確に定義された責任を持ち、相互に連携しながら医薬品や製品の品質保証と安全確保を担います。GQP省令では、この三役の組織体制が品質管理システムの基盤として重要視されています。
GQP省令に即して製造販売業者(製販)が適切な品質管理体制を運用するためには、以下の文書が最低限必要です。これらの文書は、GQP省令で求められる各項目に対応し、品質管理業務の実施と記録を確実にするために重要です。
これらの文書は、GQP省令に基づく運用を実現し、製販業者が市場に安全で有効な製品を提供するために必要不可欠です。また、文書の整備だけでなく、これらを活用した実効的な管理体制の運用も重要です。
委託先との品質取り決め書(quality agreement)など契約書には,取決めの背景や根拠法など記載する必要があり,どの法律のどの条項であるかを記載するには,以下のレジメが役に立つ.例えば,製造業者との取決めについては,GQ背省令(7条)であることが分かる.
・医薬品、医薬部外品、化粧品及び再生医療等製品の品質管理の基準に関する省令(◆平成16年09月22日厚生労働省令第136号)
これらの項目は、製造販売業者が製品の品質を確保し、市場に安全で有効な製品を提供するための基準を包括的に示しています。
GQP省令(Good Quality Practice)は、医薬品、医薬部外品、化粧品、再生医療等製品の品質管理に関する基準を定めた厚生労働省の省令です。市販後の製品に関する品質管理について規定されています。この省令は、製品の品質を確保し、消費者の安全を守るために重要な役割を果たします。以下はその主な内容です:
GQP省令は、製造販売業者が製品の品質を適切に管理し、消費者に安全で効果的な製品を提供するための指針となっています。
QP省令には品質標準書に関する記載があります。具体的には、GQP省令第5条において、製造販売業者が「品質標準書」を作成することが求められています。この品質標準書には、以下のような内容が含まれることが一般的です:
品質標準書は、製品ごとに作成される必要があり、製造販売業者が品質管理を適切に行うための重要な文書です。また、製造業者や試験機関との整合性を確保することも求められます。
品質管理手順書は、具体的な業務運用を規定する文書であり、自己点検に関連する以下の事項を記載します:
教育訓練に関連する具体的な手順や運用を記載し、従業員が正確に実行できるようにします。
文書および記録の管理について、具体的な手順や基準を定めた内容を記載します。
教育訓練に関連する具体的な手順や運用を品質管理手順書に記載し、従業員が正確に実行できるようにします。
「製品の授受」に関する具体的な手順や運用プロセスを詳細に規定し、授受業務が円滑に行われるようにします。
| 品質標準書 | 品質管理手順書 | |
| 製造販売承認事項 | 製造販売承認番号および承認日。 製品名、一般的名称、および販売名。 承認された効能効果および用法・用量。 承認された製造方法や試験方法。 承認事項に基づく品質基準(例: 成分の種類と分量)。 製造所および試験所の登録情報。 承認事項に関連する条件や注意事項。 | 不要 |
| 市場出荷管理に関する事項 | ・出荷判定の基準(試験項目と合格基準)。 ・製造販売承認事項に基づく出荷に必要な条件。 ・出荷可能とするための必要な試験結果やデータ(例:安定性試験の結果)。 ・出荷ロットごとの記録管理に必要な項目。 | ・出荷判定のための手続き(責任者の判断フローや承認方法)。 ・出荷時の試験データや文書の確認手順。 ・出荷判定を行う責任者とその役割。 ・出荷記録の保存方法や期間。 ・出荷判定中に不備があった場合の対応手順。 |
| 製造業者および試験機関との取決め | 1) 委託先の製造業者または試験機関の名称や所在地。 2)製造における製品固有の手順や基準(例:特定の製造条件や試験条件)。 3) 承認事項に関連する製造プロセスや試験項目。 4) 製品固有の品質管理項目やリスク管理事項。 5)委託先が遵守すべき要件(例:GMPまたはGLPの適用範囲)。 | 1) 委託業務を開始する際の手順(例:契約書の締結プロセス)。 2) 製造業者や試験機関との責任分担の明確化。 3) 委託先からの製造記録や試験結果の取得方法と確認手順。 4)変更が品質に影響を与える場合の連絡および承認手続き。 5) 製品の授受 6) 委託先の監査やパフォーマンス評価手順(例:定期的なGMP/GLP適合性確認)。 |
| 品質不良の処理 | (品質固有の情報) ・品質不良の報告および調査手順。 ・品質不良と判断される基準(例:規格を外れる許容範囲の定義)。 ・製品の品質に影響を与える特定の不良項目(例:外観不良、異物混入など)。 ・試験結果に基づく品質不良の分類(軽微、不良、重大)。 不良ロットの管理手法(例:隔離保存の指示)。 | (実務的な運用手順) ・品質不良が発生した場合の報告フロー(例:責任者への連絡手順、報告期限)。 ・不良品の隔離、再試験または廃棄の手順。 ・不良原因の調査手順(例:根本原因分析、ヒアリング、記録)。 ・是正措置および予防措置(CAPA)の実施方法。 ・調査および対応の記録方法(例:日時、関係者、結果の記録)。 |
| 品質不良および回収 | (製品ごとの品質不良回収基準) ・回収の判断基準(製品が品質不良であると判断される条件)。 ・回収対象となる不良の種類(例:異物混入、規格外試験結果、不適切な外観など)。 ・回収対象となる範囲(例:特定のロット、バッチなど)。 ・回収時の品質保持条件(例:製品の貯蔵や輸送に関する要件)。 | (実際の回収業務・運用プロセス) ・品質不良が発生した場合の回収計画作成の手順。 ・回収を実施する責任者とその役割。 回収に必要な関係部署との連携手順。 ・回収状況の記録方法(例:回収製品の数や回収先の特定)。 ・回収後の製品の管理(例:隔離保管、再試験、廃棄など)。 ・規制当局への報告手順(必要な場合)。 |
| 原材料および資材に関する事項 | 原材料および資材の仕様(例: 化学的、物理的、微生物学的な基準)。 原材料の供給元やメーカーに関する情報(例: 認定サプライヤーのリスト)。 資材の特性(例: 包装材料の耐久性や遮光性など)。 原材料の試験および検査項目(例: 純度試験、異物検査)。 承認された代替サプライヤーや資材の基準。 | 原材料および資材の受け入れ時の検査手順(例: 外観検査、サンプル試験)。 不適合品が発見された場合の処理方法(例: 返却、廃棄の手順)。 資材の保管方法および条件(例: 温度管理、湿度管理)。 在庫管理手順(例: 先入れ先出し(FIFO)方式の使用)。 原材料および資材のトレーサビリティ確保方法(例: ロット番号管理)。 |
| 添付文書および表示内容 | 添付文書の内容(効能効果、用法用量、副作用の記載事項など)。 表示に必要な要件(例: 有効成分の名称や分量、使用期限の記載方法)。 包装ラベルやパッケージに記載すべき特定の注意事項。 承認された表示内容や文書フォーマットに関する基準。 改訂が必要な場合の具体的条件(例: 法改正や規制当局からの指示による改訂)。 | 添付文書や表示内容の作成および改訂手順。 添付文書やラベルの確認・承認フロー(責任者の承認方法)。 表示内容の変更管理手順(例: 承認取得後の変更対応)。 添付文書や表示ラベルの印刷時のチェック手順(例: 誤記防止のためのダブルチェック手法)。 保管および配布管理(例: 印刷部数の管理、最新版の維持管理)。 |
| 変更管理および改訂履歴 | 製品に関する変更内容の具体例(例:処方、製造方法、試験方法の変更など)。 変更による品質への影響の評価結果。 承認事項に関連する変更が必要となる場合の記録。 改訂の履歴(変更の内容、改訂日、責任者など)。 | 変更の提案、承認、実施、評価に関する手順。 変更が製品品質に影響を与えるかどうかのリスク評価方法。 改訂のフロー(誰がどのように改訂を行い、承認を得るか)。 変更後の確認手順(例:製品試験やプロセスバリデーションの実施)。 改訂履歴の記録方法(保管期間や責任者の指定)。 |
| 文書および記録の管理 | 不要 | 別章を参照 |
| 自己点検 | 不要 | 別章を参照 |
| 教育訓練 | 不要 | 別章を参照 |
| その他必要な事項 |
総括製造販売責任者
2025/03/19 Mrはりきり
2025/03/20 追記(はじめに)

医薬品の品質マニュアルに関する省令は、主にGMP(Good Manufacturing Practice: 医薬品及び医療機器の製造管理及び品質管理基準)に基づいています。GMPは、医薬品の製造および品質管理に関する基準を定めており、医薬品の安全性、有効性、品質を確保するための重要な規制です。
医薬品における品質マニュアル(Quality Manual)は、製品の品質を確保し、規制要件を満たすために重要な文書です。以下のような項目が一般的に含まれます:
■参考:
医薬品の品質マニュアル作成の参考 : 000218596.pdf
医療機器や体外診断用医薬品の参考 : 品質マニュアル(QMS省令2021年版対応)

今から8年後になるんだけど大阪モノレールが延長されて寝屋川から横切る近鉄線を一つ越え瓜生まで開通する。この工事状況を横目に「らんぷ」に来た。
モーニングは12時までやってる。エッグトースト、美味しいよ。


炎のテクスチャを作る方法についてCopilotに2つの質問をした.copilotは,古い情報から答えることもあるので,得られる回答は鵜呑みにしないで,概要的な説明であることを理解して,現在の環境やblenderのバージョンに沿った個々の確認が必要である.
以下,Copilotの回答は,おおよその方向性を示していることは初心者にとって本当に助かるが.今後の確認のための作業は,先人達が歩いた痕跡を辿るわけで,それはそれで骨の折れる作業となる.確認が取れれば追記・修正する.
Copilot : Blenderのシェーダーノードを使用してマッチの炎を表現するには、ノードの組み合わせを活用してリアルな炎の動きや色合いを作成できます。以下の手順を参考にしてください。
#frame * 0.1 のような式を用いることで時間に応じた自然な変化を表現できます。もし特定の部分でつまずいたり、さらに詳細が必要でしたらお気軽に教えてください。楽しい制作を応援しています! 🔥
下のnode図の緑色網掛けがvalue nodeで,この値をスライドさせると模様が正方向/逆方向に流れていくのを見ることが出来る.
その値とaminmationのタイムラインを関連づけると,スペースキーでアニメーションを見ることが出来る.

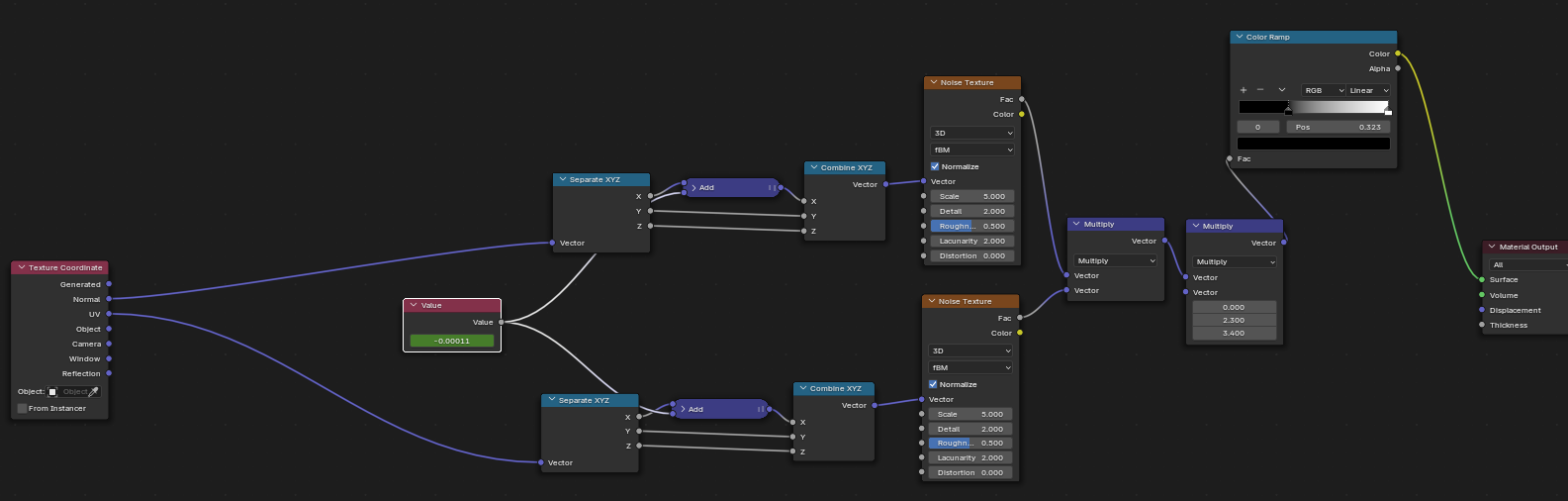
参考 : (338) Anime Style Procedural Fire in Blender 2.8 – YouTube
Copilot : Blenderで「マスキング」を活用することで、特定の範囲だけテクスチャやシェーダーの効果を適用することができます。これには、ノードを使った設定が便利です。以下に、マスキングを具体的に行う方法を説明します。
Gradient Texture 出力を「Greater Than」に接続して、特定の閾値でマスクを作成。マッチの炎のテクスチャでは、炎の形状や動きをリアルにするためにノイズとグラデーションを使ったマスクが非常に効果的です。以下のように組み合わせます:
Noise Textureを追加して炎のゆらぎを再現し、それをColor Rampと組み合わせて形状を調整。
下部(炎の根元)は黄色や白で鮮明にし、上に行くほど暗くフェードアウト。
Gradient Textureノードを使い、炎の高さ方向に対するマスクを作成。
![QoL – 睡眠時無呼吸症候群の確定診断を受けてからもう10年が経過したが,当初はダイエット,最近では文明の利器を使って改善を模索してきた[2025/03/15].](https://harikiri.diskstation.me/myblog/wp-content/uploads/2021/02/80F3D755-3019-49C6-BDAE-47D137C87826.jpeg)
年を取ってくるとクオリティーオブライフ(QoL)を高めたい.若い頃は勢いで乗り越えてきたが,これからはそうもいかない.
2015年9月に家族の進めで睡眠時無呼吸症候群の診断のために一泊二日で検査入院をしてから,もう10年も経過してしまった.その結果は,血中酸素濃度が90%を軽く下回ってしまうポイントがあり重症の「睡眠度無呼吸症候群」であると確定診断された.その後,病院からの処方により睡眠時にCPAPを付けて寝るようにしたが,かえって息苦しく1週間で挫折した.
その後,就寝時に「ナステント」という鼻から口蓋のとこまで挿入するシリコンチューブの医療用機器(?)を試してみた.この頃は,Apple Watchを持っていなかったので装着でのモニタリングは無く自覚的な感想になる.まぁ,呼吸はできていた!.僕の場合,口蓋が鼻を塞ぐことが主な現象なので,そこにチューブが入っていると塞がらないことが理由と考えられる.
ナステントも経済的にバカにならないので,洗浄して再使用したりしていたが,その内に使わなくなった.
一方,一時期流行った「バターコーヒー」によるダイエットの効果があり5Kgの減量となったことで無呼吸も楽になった.
睡眠時に頻繁な無呼吸になると色々な体の機能を犯すと考えられている.因果関係は分からないが,血中尿素窒素や尿酸が上限ギリギリで若い頃から維持していたのだが,手指の関節が痛くなり検査の結果,血中尿素窒素(正常範囲7.0)が8を超えたことから,その合成阻害剤を処方され長期の服用を続けていた(最近は停止中,これまでになんどが投薬の停止を試みている).
2018年には突発性難聴.2019年には持病の白内障が視力的にこれ以上の無処置は不可能となり,レンズを交換した.その後,白内障の手術をするとコンプライアンスが悪くなることで,その他の目の不具合も起こしやすくなるとは聞いていたが,2021年頃からは緑内障(三日月の影が視野の上に見えてきた)が,眼圧は正常班内であったので正常眼圧緑内障と診断された.とりあえず,眼圧を下げておくことは悪い影響はないとのことで,現在(2025/3)まで使用してきた.しかし,視野範囲の減少速度は低下せず点眼薬の効果はほとんど無いと感じている.
それで思うことは,点眼に頼り過ぎていたのではないか(朝にプリモジン,昼過ぎ : プリモジン,夜 : タプロス).他に力点を移す方が良いのではないか.そんな訳で,この点眼ももういいか.と思い始めた.
あと,年齢もあるのだが,頭髪減少も進行中である.睡眠時の酸素欠乏は頭髪にも影響していることは高い確率で言えるものと思っている.
最近,考え方を少し変えてきていることは前述しているが,血中尿素窒素(尿酸)の合成阻害薬である「フェブリク」やジェネリック医薬品は,もういいかと.尿酸が高いことで,その結晶が関節に傷をつけて痛風になったり,痛風腎になったりするのだが,62歳を過ぎてもういいかと思ってきている.尿酸は,抗酸化剤であり高いことは全てに悪い影響であるとは言えないため,抗酸化の効果を期待して,緑内障による視神経を損傷の原因は,酸素欠乏や若しくは酸化による炎症など,何れが原因かはわからないが,点眼を継続してきたこの数年での視野狭窄の進行が減衰していない.フェブリクなどは服用しないことにした.その理由は,抗酸化効果が尿酸の効果を期待ともういいかの心境からである.
尿酸合成阻害剤の服用を停止してから,もう1カ月は経過しているが,10日経過時点の健康診断の結果,血中尿酸値は上限ギリギリ(7.1)であった.関節がいたくないのてら,ここままいくことにしようと思う.
あと,睡眠時無呼吸が万病のものとであとの認識から対策していることは,昨年の口蓋へのレーザー治療を10回(10カ月程度)の施術を実行した.同時期に,寝具のテンピュールが発表・発売しているいびきを感知してベッドが傾斜するというベッド(Zero-G)を使用して毎日の睡眠を継続している.日々の睡眠のモニタリングにはApple Watchにより血中酸素濃度,心拍数,ベッドの機能である覚醒や深い睡眠のイベント記録,iPhoneのアプリであるい「びきラボ」によるいびきの記録,である.これらを使って毎日の複数の記録を付き合わせて検討している.

最近,その別途の設定で良い条件を見つけた.結集酸素濃度も極端に低くならないし,いびきは,いびきラボの数値として一桁(状態が悪い時のいびき指数は70を超えたこともある.通常は30程度)になった.その条件項目として頭の角度,腰および足の角度であるが,頭の角度を上げると,体がベッドの脚の方に下がってくるのが常.そごて足の角度を上げてやるのだか,寝やすさの兼ね合いもあってそれぞれの角度の値と組み合わせは試行錯誤が必要であった.
枕も試行錯誤をしてきたが,結局は高価な枕は必要ない.イオンで1,000程度のプラスチック綿の枕を使用しているが高さはなく低い.一工夫している点は,枕をそのままベッドの上に置いた状態で仰向けになり両手を上げて枕の両端を持ち,頭を上げてクルリと90℃回転させて首の位置70%,頭の位置30%で頭を枕に降ろしていく.首には隙間が無いようにして首の負担を減らすことが理想.頭を完全に落とすと,両端の枕の角(耳)は自分の耳を塞ぐように接近してくる.これで音も静かにやり首も楽になる.これはZero-Gとの併用である.
この設定で,もうしぱらく観察することにしよう.
今使っているApple WatchはSerise 6だが,最近のSerise 9, 10やUltra 2では,睡眠時無呼吸症候群を検知できるらしい.これはまた今度にしよう.
以上,殴り書いたが,また更新を予定している.
2025/03/15 Mrはりきり

最終兵器彼女/TVシリーズは2002年の全13話作品.舞台背景は北海道.Amazon primeのアニメタイムズで一気に視聴(2025/03/05)した.製作はGONZO DIGIMATION.GONZOはこの辺りの時代の作品に何度かみかけたことがある.英語のタイトルは,THE LAST LOVE SONG ON THIS LITTLE PLANET.」だが,うむ,英語のタイトルは,内容を示唆しているようにも思う.
エンドロールに方言指導の記載もあるが,なかなかよく演出されている.北海道での生活を思い出しながら、かたや懐かしく試聴した。
背景は,日本での戦争を前提にした若者たちの選択を描くもので決してハッピーエンドではなく,トラウマになりそうだったが,良くも悪くも僕には強烈な印象を与えた.
2025/03/15 Mrはりきり